Chỉ dùng thêm 1 kim loại phân biệt các dung dịch :NaCl ,MgCl2 , FeCl2 , FeCl3 , CuSO4 , (NH4)2SO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phương pháp: thử 5 hóa chất hữu dụng: Ba(OH)2, H2SO4, AgNO3, Quì, HCl
|
|
NH4Cl |
(NH4)2SO4 |
NaNO3 |
| Ba(OH)2 |
↑NH3 Mùi khai |
↑NH3 Mùi khai BaSO4 ↓trắng |
x |
|
|
MgCl2 |
FeCl2 |
FeCl3 |
|
|
Mg(OH)2 Trắng |
Fe(OH)2 xanh |
Fe(OH)3 Nâu đỏ |
|
|
Al(NO3)3 |
|
|
|
|
Al(OH)3 Trắng sau đó tan dần |
|
|

1. Cho HNO3 tác dụng với từng chất:
- Có tác dụng -> Na2CO3
- Không tác dụng -> AgNO3, KNO3
Cho từng chất tác dụng với Na2CO3 vừa nhận biết được:
- Có tác dụng -> AgNO3
- Không tác dụng -> KNO3
2. Cho H2SO4 tác dụng với từng chất:
- Có tác dụng:
+ Kết tủa trắng -> BaCl2
+ Có khí không màu, mùi hắc thoát ra -> K2SO3
- Không tác dụng -> NaCl
3. Cho thử quỳ tím:
- Đổi màu xanh -> Ba(OH)2
- Đổi màu đỏ -> HCl, H2SO4 (1)
- Không đổi màu -> NaCl, K2SO3 (2)
Cho từng chất (1) tác dụng với từng chất (2), có 2 cặp chất tác dụng với nhau:
- HCl và K2SO4
- NaCl và H2SO4

Dùng dung dịch Ba(OH)2 dư
+ Có mùi khai : NH4NO3
2NH4NO3 + Ba(OH)2 → Ba(NO3)2 + 2H2O + 2NH3
+ Có mùi khai và có kết tủa trắng : (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 → 2NH3 + 2H2O + BaSO4↓
+ Kết tủa màu xanh lam và kết tủa trắng : CuSO4
Ba(OH)2 + CuSO4 → Cu(OH)2↓ + BaSO4↓
+ Kết tủa nâu đỏ : Fe(NO3)3
2Fe(NO3)3 + 3Ba(OH)2 → 2Fe(OH)3↓ + 3Ba(NO3)2
+ Kết tủa trắng xanh lá cây : FeCl2
Ba(OH)2 + FeCl2 → BaCl2 + Fe(OH)2↓
+Kết tủa trắng: MgCl2
MgCl2 + Ba(OH)2 → Mg(OH)2 ↓ + BaCl2
+ Kết tủa keo trắng sau đó tan dần : AlCl3
2AlCl3 + 3Ba(OH)2 ⟶ 2Al(OH)3 + 3BaCl2
2Al(OH)3 + Ba(OH)2 → Ba(AlO2)2 + 4H2O
+Không hiện tượng : NaCl
Dung dịch màu xanh là CuSO4, màu lục nhạt là FeCl2
- Đổ dd KOH dư vào từng dd còn lại
+) Xuất hiện kết tủa lâu đỏ: Fe(NO3)3
PTHH: \(3KOH+Fe\left(NO_3\right)_3\rightarrow3KNO_3+Fe\left(OH\right)_3\downarrow\)
+) Xuất hiện kết tủa trắng: MgCl2
PTHH: \(MgCl_2+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+2KCl\)
+) Xuất hiện kết tủa keo rồi tan: AlCl3
PTHH: \(AlCl_3+3KOH\rightarrow3KCl+Al\left(OH\right)_3\downarrow\)
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
+) Xuất hiện khí: NH4NO3 và (NH4)2SO4
PTHH: \(NH_4NO_3+KOH\rightarrow KNO_3+NH_3\uparrow+H_2O\)
\(2KOH+\left(NH_4\right)_2SO_4\rightarrow K_2SO_4+2NH_3\uparrow+2H_2O\)
- Đổ dd BaCl2 vào 2 dd còn lại
+) Xuất hiện kết tủa: (NH4)2SO4
PTHH: \(\left(NH_4\right)_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NH_4Cl\)
+) Không hiện tượng: NH4NO3

Chọn D.
- Dùng dung dịch KOH ta có kết quả:
CuCl2: xuất hiện kết tủa xanh; FeCl3: xuất hiện kết tủa nâu đỏ; FeCl2: xuất hiện kết tủa trắng xanh.
NH4Cl: sủi khí mùi khai; AICl3 xuất hiện kết tủa keo trắng, sau đó tan trong NaOH dư.
MgCl2: xuất hiện kết tủa trắng; NaOH, NaCl: không hiện tượng.
- Dùng AlCl3 nhận biết ở trên, nhận NaOH và NaCl.

chọn Ba(OH)2
MgCl2 + Ba(OH)2 → BaCl2 + Mg(OH)2 kết tủa trắng Ba(OH)2 + CuCl2 → BaCl2 + Cu(OH)2 kết tủa xanh FeCl2 + Ba(OH)2 → BaCl2 + Fe(OH)2 có cả kết tủa trắng và xanh 3Ba(OH)2 + 2FeCl3 → 3BaCl2 + 2Fe(OH)3 kết tủa nâu đỏ 2AlCl3 + 3Ba(OH)2 → 2Al(OH)3 + 3BaCl2 kết tủa keo trắng 2NH4Cl + Ba(OH)2 → BaCl2 + 2H2O + 2NH3 giải phóng khí có mùi khai (NH4)2SO4 + Ba(OH)2 → H2O + 2NH3 + BaSO4 khí có mùi khai bay lên, tạo kết tủa trắng không có hiện tượng là NaCl
Đáp án D
A. Sai. Không thể sử dụng kim loại K để nhận biết các dung dịch trên vì khi cho kim loại K vào dung dịch, K sẽ tác dụng với nước tạo thành KOH, khi đó có hai dung dịch (NH4)2SO4 và NH4NO3 có cùng hiện tượng là có khí không màu có mùi khai thoát ra.
B. Sai. Không thể sử dụng dung dịch NaOH để nhận biết các dung dịch trên vì có hai dung dịch (NH4)2SO4 và NH4NO3 có cùng hiện tượng là có khí không màu có mùi khai thoát ra.
C. Sai. Không thể sử dụng dung dịch BaCl2 để nhận biết các dung dịch trên vì có bốn dung dịch CuSO4, Al2(SO4)3, Na2CO3 và (NH4)2SO4 có cùng hiện tượng là xuất hiện kết tủa trắng.
D. Đúng. Có thể sử dụng kim loại Ba để nhận biết các dung dịch trên vì khi cho kim loại Ba vào dung dịch, Ba sẽ tác dụng với nước tạo thành Ba(OH)2, khi đó:
+ Mẫu thử nào có kết tủa màu xanh lam xuất hiện → Mẫu thử đó là CuSO4 (thực tế là hỗn hợp kết tủa Cu(OH)2 màu xanh lam và BaSO4 màu trắng lẫn vào nhau).
Ba(OH)2 + CuSO4 → BaSO4↓ + Cu(OH)2↓
+ Mẫu thử nào có kết tủa màu trắng hơi xanh, sau đó chuyển dần sang nâu đỏ → Mẫu thử đó là FeCl2.
+ Mẫu thử nào có kết tủa màu trắng xuất hiện (thực tế là hỗn hợp kết tủa Al(OH)3 màu trắng keo và BaSO4 màu trắng), sau đó khi cho lượng Ba đến dư vào thì lượng kết tủa tan một phần và còn lại phần kết tủa trắng không tan → Mẫu thử đó là Al2(SO4)3.
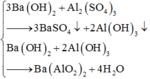
+ Mẫu thử nào có kết tủa trắng xuất hiện → Mẫu thử đó là Na2CO3.
Ba(OH)2 + Na2CO3 → BaCO3↓ + 2NaOH
+ Mẫu thử nào có kết tủa màu trắng xuất hiện đồng thời có khí không màu có mùi khai thoát ra → Mẫu thử đó là (NH4)2SO4.
Ba(OH)2 + (NH4)2SO4 → BaSO4↓ + 2NH3 + 2H2O
+ Mẫu thử nào có khí không màu có mùi khai thoát ra → Mẫu thử đó là NH4NO3.
Ba(OH)2 + 2NH4NO3 → Ba(NO3)2 + 2NH3 + 2H2O

dùng Ba
Ba + 2H2O ---> Ba(OH)2 + H2 (khí không màu, xuất hiện trong mọi phản ứng)
+ không hiện tượng (chỉ có khí không màu bay lên): NaCl
+ có khí không màu, đồng thời xuất hiện kết tủa trắng: MgCl2
MgCl2 + Ba(OH)2 ---> BaCl2 + Mg(OH)2 (trắng)
+ có khí không màu, đồng thời xuất hiện kết tủa trắng xanh: FeCl2
FeCl2 + Ba(OH)2 ---> BaCl2 + Fe(OH)2 (trắng xanh)
+ có khí không màu, đồng thời xuất hiện kết tủa nâu đỏ: FeCl3
2FeCl3 + 3Ba(OH)2 ---> 3BaCl2 + 2Fe(OH)3 (nâu đỏ)
+ có khí không màu, 1 kết tủa trắng và 1 kết tủa xanh lơ: CuSO4
CuSO4 + Ba(OH)2 ---> Cu(OH)2 (xanh lơ) + BaSO4 (trắng)
+ có khí có mùi khai, kết tủa trắng xuất hiện: (NH4)2SO4
(NH4)2SO4 + Ba(OH)2 ---> BaSO4 (trắng) + 2NH3 (khí mùi khai) + 2H2O