một hỗn hợp gồm 3 kim loại Na,Al,Fe Nếu cho hỗn hợp đó vào nước đến khi phản ứng xong thu được V lít khí . Nếu cho lượng hỗn hợp đó vào dung dịch NaOH dư đến khi phản ứng xong thu được 7/4 V lít khí . Nếu cho lượng hỗn hợp đó vào dung dịch HCl dư đến khi phản ứng xong thu được 9/4 V lít khí ( đktc) a. Viết PTHH b. Tính % khối lượng mỗi chất trong hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : D
Gọi số mol Mg = Fe = x ; số mol Al = y ; số mol Cu = z trong X
=> 80x + 27y + 64z = 7,5g
2 n H 2 = 2nMg + 2nFe + 3nAl
=> 4x + 3y = 0,46 mol
Khi cho 1 lượng vừa đủ Mg(NO3)2 để phản ứng với Cu và Fe2+
tạo khí không màu hóa nâu trong không khí (NO)
=> NO3- chuyển hoàn toàn thành NO
=> bảo toàn e : 2nCu + n F e 2 + = 3nNO = 3 n N O 3
=> n N O 3 = (2z + x)/3 mol
=> n M g N O 3 2 = (x + 2z)/6 (mol)
=> Khi phản ứng với NaOH tạo kết tủa gồm :
x mol Fe(OH)3 ; [x + (x + 2z)/6 ] mol Mg(OH)2 và z mol Cu(OH)2
=> 9,92g = 524x/3 + 352z/3
=> x = 0,04 ; y = 0,1 ; z = 0,025 mol
=>%mFe(X) = 29,87%

Xét phản ứng (2) và (3) ta có: $n_{Fe}=\frac{9a}{4}-\frac{7a}{4}=\frac{a}{2}(mol)$
Gọi số mol Na và Al lần lượt là x;y
Xét phản ứng (1):
$2Na+2H_2O\rightarrow 2NaOH+H_2$
$2Al+2NaOH+2H_2O\rightarrow 2NaAlO_2+3H_2$
$\Rightarrow n_{H_2}=a=2x\Rightarrow n_{Na}=\frac{a}{2}(mol)$
Xét phản ứng (2) bảo toàn e ta có:
$n_{Al}=y=\frac{5a}{6}(mol)$
$\Rightarrow n_{Na}:n_{Al}:n_{Fe}=3:5:3$

Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 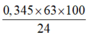
= 90,5625 gam

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam

Bắt đầu xuất hiện kết tủa nghĩa là: NaOH đầu tiên sẽ trung hòa HCl dư trước
NaOH + HCldư → NaCl + H2O
0,2 ←0,2
→ 2V1 = 0,2 → V1 = 0,1
Đến khi kết tủa không thay đổi khối lượng thì khi đó kết tủa bị hòa tan hết.
3NaOH + AlCl3 → 3NaCl + Al(OH)3↓
3x ←x → x
NaOH + Al(OH)3 → NaAlO2 + 2H2O
x ←x
→ 0,2 + 4x = 0,6.2 → x = 0,25
=> y = 0,025
=> m = 17,75g

Đặt \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Na}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
a--------------------------->a
\(2Na+2HCl\rightarrow2NaCl+H_2\)
b---------------------------->0,5b
Ta có: \(m_M=\dfrac{1}{2}.\left(m_{Fe}+m_{Na}\right)=\dfrac{1}{2}.\left(56a+23b\right)=28a+11,5b\left(g\right)\)
PTHH: \(M+2HCl\rightarrow MCl_2+H_2\)
(a+0,5b)<----------------(a+0,5b)
\(\Rightarrow M_M=\dfrac{28a+11,5b}{a+0,5b}\\ \Rightarrow\dfrac{28a}{a}>M_M>\dfrac{11,5a}{0,5a}\\ \Leftrightarrow28>M_M>23\)
Vậy M là Magie (Mg)

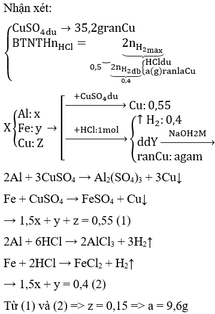
Giải thích:
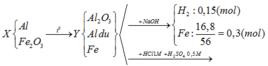
BT e: nAl dư = 2/3 nH2 = 2/3. 0,15 = 0,1 (mol)
BTNT: Fe => nFe2O3 = ½ nFe = 0,15 (mol)
Phản ứng xảy ra hoàn toàn, Al dư sau phản ứng ( vì Y + NaOH có khí H2 bay ra), do đó Fe2O3 phản ứng hết
Fe2O3 + 2Al Al2O3 + 2Fe
0,15 → 0,3
=> nAl ban đầu = 0,3 + 0,1 = 0,4 (mol)
nHCl = V (mol) ; nH2SO4 = 0,5V (mol)
Bảo toàn điện tích khi cho Y tác dụng với hh axit
=> 2nFe2+ + 3nAl3+ = nCl- + 2nSO42-
=> 2.0,3 + 3. 0,4 = V + 2. 0,5V
=> V = 0,9 (lít)
Đáp án B

I. Nội qui tham gia "Giúp tôi giải toán"
1. Không đưa câu hỏi linh tinh lên diễn đàn, chỉ đưa các bài mà mình không giải được hoặc các câu hỏi hay lên diễn đàn;
2. Không trả lời linh tinh, không phù hợp với nội dung câu hỏi trên diễn đàn.
3. Không "Đúng" vào các câu trả lời linh tinh nhằm gian lận điểm hỏi đáp.
Các bạn vi phạm 3 điều trên sẽ bị giáo viên của Online Math trừ hết điểm hỏi đáp, có thể bị khóa tài khoản hoặc bị cấm vĩnh viễn không đăng nhập vào trang web.
a,
2NaOH + 2H2O ---> 2NaOH + H2
Al + NaOH + H2O ---> NaAlO2 + H2
2Na + 2HCl ---> 2NaCl + H2
Fe + 2HCl ---> FeCl2 + H2
2Al + 6HCl ---> 2AlCl3 + 3H2