Hãy trình bày sự nhiệt phân muối vô cơ ( muối hiđrocacbonat và cacbonat ; muối nitrat ; muối amoni ; muối gốc axit ko có oxi)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nCO2 = 10,08/22,4 = 0,45 (mol)
PTHH: CaCO3 -t°-> CaO + CO2
0,45 0,45 0,45
mCO2 = 0,45 . 44 = 19,8 (g)
mCaCO3 = 0,45 . 100 = 45 (g)
mCaO = 0,45 . 56 = 25,2 (g)
Số phân tử CaCO3 = CaO: 0,45 . 6.10^23 = 2,7.10^23 (phân tử)

nCaO = 7/56 = 0,125 (mol)
PTHH: CaCO3 -t°-> CaO + CO2
0,125 0,125 0,125
mCaCO3 = 0,125 . 100 = 12,5 (g)
Số phân tử CaCO3 = CO2: 0,125 . 6 . 10^23 = 0,75.10^23 (phân tử)
mCO2 = 0,125 . 44 = 5,5 (g)
VCO2 = 0,125 . 22,4 = 2,8 (l)

Muối cacbonat --phân huỷ--> CaO => muối đó là CaCO3
\(a,n_{CaO}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\uparrow\)
0,15<----0,15
\(b,m_{CaCO_3}=0,15.100=15\left(g\right)\)

PT: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
Ta có: \(n_{CaCO_3}=\dfrac{2,1.10^{24}}{6.10^{23}}=3,5\left(mol\right)\)
a, Theo PT: \(n_{CaO}=n_{CO_2}=n_{CaCO_3}=3,5\left(mol\right)\)
\(\Rightarrow A_{CaO}=A_{CO_2}=3,5.6.10^{23}=2,1.10^{24}\) (phân tử)
b, \(m_{CaO}=3,5.56=196\left(g\right)\)
\(m_{CO_2}=3,5.44=154\left(g\right)\)
c, \(V_{CO_2}=3,5.24,79=86,765\left(l\right)\)

Đáp án A
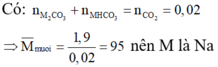
(Trong hỗn hợp cần có 1 muối có khối lượng mol lớn hơn và 1 muối có khối lượng mol < 95)

\(Đặt:ACO_3\\ ACO_3\underrightarrow{to}AO+CO_2\\ n_{CO_2}=\dfrac{3,5-1,96}{44}=0,035\left(mol\right)\\ \Rightarrow n_{ACO_3}=0,035\left(mol\right)\\ \Rightarrow M_{ACO_3}=\dfrac{3,5}{0,035}=100\left(\dfrac{g}{mol}\right)\\ Mà:M_{ACO_3}=M_A+60\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_A+60=100\\ \Leftrightarrow M_A=40\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Canxi\left(Ca=40\right)\\ Muối:CaCO_3\)
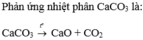

1. Muối hiđrocacbonat (HCO3) và cacbonat (CO3)
- Sơ đồ chung:
2M(HCO3)n ----t1----> M2(CO3)n + CO2 + H2O
M2(CO3)n ---t2--> M2On + nCO2 (t1 << t2)
VD. Ca(HCO3)2 → CaCO3 + CO2 + H2O (đk: to)
- Ở nhiệt độ t1 chỉ cần đun nóng dd là phân hủy.Riêng muối của kim loại kiềm và amoni thì phải nung khan mới phân hủy
* Nhiệt phân muối cacbonat axit
Ca(HCO3)2 -> CaCO3 + CO2 + H2O (đk: to)
Mg(HCO3)2 -> MgCO3 + CO2 + H2O (đk: to)
2NaHCO3 -> Na2CO3 + CO2 + H2O (đk: to)
- Ở nhiệt độ t2 kim loại càng mạnh thì phải nung ở nhiệt độ càng cao. Riêng muối của kim loại kiềm xem như ko bị phân hủy
* Nhiệt phân muối cacbonat trung hòa ko tan
CaCO3 -> CaO + CO2 (to)
MgCO3 -> MgO + CO2 (to)
FeCO3 -> FeO + CO2 ( ko có ko khí) (to)
4FeCO3 + O2 -> 2Fe2O3 + 4CO2 (có ko khí) (to)
2. Muối hiđrosunfit (HSO3) và sunfit (SO3)
-Các muối này bền vs nhiệt hơn các muối trong trường hợp 1, tuy nhiên quy luật nhiệt phân cx giống như phần 1
3. Muối nitrat (NO3)
-Tất cả các muối nitrat đều bị nhiệt phân, sản phẩm nhiệt phân tùy thuộc vào mức độ hoạt động của kim loại
- Muối nitrat của kim loại hoạt động mạnh K, Na, Ba, Ca,...
M(NO3)n → M(NO2)n + \(\dfrac{n}{2}\)O2 (đk: to)
VD. Ca(NO3)2 -> Ca(NO2)2 + O2
2KNO3 -> 2KNO2 + O2
- Muối nitrat của kim loại hoạt động trung bình từ Mg....Cu ---to--> oxit kim loại hóa trị cao + NO2 + O2
VD. Cu(NO3)2 ---to---> CuO + 2NO2 + 1/2O2
-Muối nitrat của kim loại hoạt động yếu (sau Cu)
M(NO3)n ---to---> M + nNO2 + \(\dfrac{n}{2}\)O2
VD. AgNO3 -to---> Ag + NO2 + \(\dfrac{1}{2}\)O2
-Chú ý: Khi nhiệt phân muối nitrat mà sản phẩm là khí và hời thì đó là các muối nitrat sau:
NH4NO3 ---to--> NO2 + 2H2O
Hg(NO3)2 ---to--> Hg(l) + 2NO2 + \(\dfrac{1}{2}\)O2 ; Hg(l) ---to--> Hg(h)
- Thuốc nổ đen là hh 75% KNO3 , 10% S và 15% C theo khối lượng
Phản ứng nổ: 2KNO3 + 3C + S ---to--> K2S + 3CO3 + N2
4. Muối amoni (NH4)
-Tất cả các muối amoni đều bị nhiệt phân
-Muối amoni của axit dễ bay hơi (HCl ,H2CO3, H2S,...) → NH3 + axit tương ứng
VD. NH4HCO3 ---to--> NH3 + CO2 + H2O
(NH4HCO3 dùng lm bột nở trong bánh)
NH4Cl ---to--> NH3 + HCl
-Muối amoni của axit HNO3, HNO2
NH4NO2 ---to--> N2 + 2H2O
NH4NO3 ---to--> N2O + 2H2O
NH4NO3 ---to cao--> N2 + \(\dfrac{1}{2}\)O2 + 2H2O
5. Muối gốc axit ko có oxi
- Hầu hết các muối gốc axit ko chứa oxi ko bị nhiệt phân hủy. Riêng muối AgCl rất nhạy vs ánh sáng
2AgCl ----ag----> 2Ag + Cl2 (pư quang hóa)
-Các muối sunfua cx ko bị nhiệt phân nhưng rất dễ cháy tạo ra oxit kim loại hóa trị cao và SO2
VD. 4FeS2 + 11O2 ---to--> 2Fe2O3 + 8SO2
2CuS + 3O2 ---to--> 2CuO + 2SO2
4FeS + 7O2 ---to--> 2Fe2O3 + 4SO2
Cu2S + 2O2 ---to--> 2CuO + SO2
6.Muối halogen có oxi (p/s: các này bn ko yêu cầu mik ghi nhưng mik nghĩ chắc bn cx sẽ cần ^^)
KClO3 ---to MnO2 --> KCl + \(\dfrac{3}{2}\)O2 (chủ yếu)
4KClO3 ---to-->KCl + 3KClO4
P/s: Sắp gãy tay rồi -.- Mất gần 30' của mik đó....Bài này ko dc tick chắc ngồi khóc =)) Xem lại kĩ pthh xem mik có cân bằng đúng chưa nha...vội vàng sợ chưa cân :)
Bổ sung thêm muối hiđrosunfit và sunfit nữa nha