cho m(g) khí CO2 sục vào 100ml dung dịch Ca(OH)2 0,05M thu được 0,1g chất không tan tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CaCO_3}=\dfrac{0,1}{100}=0,001\left(mol\right)\)
nCa(OH)2 = 0,5.0,01 = 0,005(mol)
TH1: Chỉ tạo ra muối trung hòa
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
_____________0,001<---0,001
=> m = 0,001.44 = 0,044 (g)
TH2: Có tạo ra muối axit
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
_____0,005---->0,005---->0,005
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,004--->0,004
=> m = (0,005+0,004).44 = 0,396(g)

\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{KOH}=0,8.0,05=0,04\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,02.0,8=0,016\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3\(\downarrow\) + H2O
______0,016---->0,016---->0,016___________(mol)
2KOH + CO2 --> K2CO3 + H2O
0,04--->0,02----->0,02_____________________(mol)
K2CO3 + CO2 + H2O --> 2KHCO3
0,004<---0,004----------->0,008_______________(mol)
mCaCO3 = 0,016.100 = 1,6 (g)
A chứa K2CO3: 0,016 mol và KHCO3: 0,008 mol
\(\left\{{}\begin{matrix}C_{M\left(K_2CO_3\right)}=\dfrac{0,016}{0,8}=0,02M\\C_{M\left(KHCO_3\right)}=\dfrac{0,008}{0,8}=0,01M\end{matrix}\right.\)

Đáp án : D
Ta có : n CaCO3 = 7,5 /100 = 0,075 mol
n Ca(OH)2 = 0,1 mol
ta thấy : nCaCO3 ≠ nCa(OH)2 => có 2 trường hợp
TH1 : chỉ xảy ra phản ứng tạo CaCO3 và Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
=> VCO2 = 0,075.22,4 = 1,68 lít
TH2 : xảy ra 2 phản ứng tạo muối CaCO3và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 0,025
=> tổng nCO2 = 0,075 + 0,05 = 0,125 mol
=> VCO2 = 0,125.22,4 = 2,8 lít
=> Đáp án D
CÁCH KHAC : Sử dụng phương pháp đồ thị
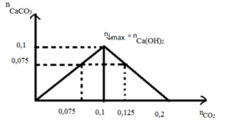
Dựa vào đồ thị => n CO2 = 0,075 mol hoặc n CO2 = 0,125 mol
=> VCO2 = 0,075.22,4 =1,68 lít hoặc VCO2 = 0,125.22,4 = 2,8 lít

Na2CO3 + HCl = NaCl + NaHCO3
KHCO3 + HCl = KCl +CO2 + H2O
n HCl = 0,1 * 1,5=0,15 mol
n CO2 = 1,008 / 22,4 =0,045 mol => n KHCO3 = 0,045 mol = n iôn K+ = n iôn HCO3 -=> nồng độ MOl
dd B tác dụng với Ba(OH)2 dư : Ba(OH)2 (dư) + NaHCO3 = BaCO3 + NaOH +H2O
n kết tủa= n BaCO3 = 29,55/197=0,15 mol => n NaHCO3 = 0,15 mol = nNa2CO3 => n Na + trong ddA = 0,15 *2 = 0,3 mol => nồng độ mol
nHCO3 - = 0,15 mol => nồng độ mol
Có n Na2CO3 và nKHCO3 dễ dàng tính được a(g)
**** Cho từ từ DD A gồm Na2CO3 và NaHCO3 va ddHCl thì sẽ có 2 trường hợp
TH1: Na2CO3 phản ứng trước:
Na2CO3 +2 HCl =2NaCl + H2O +CO2
.................0,15
n Na2CO3 ở câu trên tính dc là 0,15 mol => n HCl phản ứng ở đây là 0,15 * 2 = 0,3 mol
nCa(OH)2 = 0,005 mol
nCaCO3 = 0,001 mol
Do nCa(OH)2 > nCaCO3
Nên xảy ra 2 trường hợp
* TH1: tạo muối trung hòa ( kiềm dư )
CO2 + Ca(OH)2\(\rightarrow\) CaCO3 + H2O
\(\Rightarrow\) mCO2 = 0,001.44 = 0,044 (g)
* TH2: tạo 2 muối
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O
2CO2 + Ca(OH)2 \(\rightarrow\) Ca(HCO3)2
\(\Rightarrow\) nCO2 = 0,001 + ( 0,004.2 ) = 0,009 (mol)
\(\Rightarrow\) mCO2 = 0,009.44 = 0,396 (g)