Cho m gam kim loại Na vào 200ml dung dịch hỗn hợp gồm H2SO4 1M và HCl 2M, sau phản ứng kết thúc thu được dung dịch D và V lít khí H2 ( ở đktc). Dung dịch D hòa tan vừa đủ 7,8 gam Al(OH)3.
1. Viết các phương trình phản ứng xảy ra. Biết muối tạo thành là muối trung hòa.
2. Tính giá trị m và V.
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

31 tháng 5 2018
Đáp án A
Các phương trình phản ứng:
Dung dịch H2SO4 20% thuộc loại dung dịch loãng.
Phương trình phản ứng:
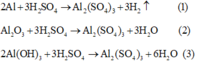
Do các chất tác dụng vừa đủ với nhau
=> dung dịch sau chỉ có chất tan là Al2(SO4)3.
Tính toán:
Ta có: n H 2 = 5 , 04 22 , 4 = 0 , 225 mol
Sơ đồ phản ứng:
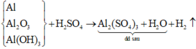
Khối lượng Al2(SO4)3 trong dung dịch sau là:
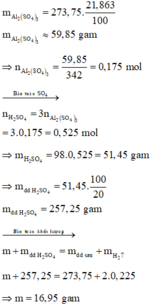






2Na + H2SO4 --> Na2SO4 +H2 (1)
2Na+ 2HCl --> 2 NaCl + H2 (2)
2Na +H2O --> 2NaOH +H2 (3)
NaOH +Al(OH)3 --> NaAlO2 +2H2O (4)
nAl(OH)3=0,1(mol)
nH2SO4=0,2(mol)
theo (4) : nNaOH=nAl(OH)3=0,1(mol)
theo (1,2,3) : nH2=0,5(mol)
=>V=11,2(l)
nNa=0,9(mol)=>m=20,7(g)
Lê Đình Thái em bổ sung thêm TH2 nhé
Đề này sẽ có 2 trường hợp:
TH1: Na td với H2O sinh ra NaOH. Axit pứ hết với NaOH, NaOH còn dư tác dụng với Al(OH)3.
TH2: NạOH phản ứng hết, axit còn dư. Axit tác dụng với Al(OH)3.