cho 28,8 gam hỗn hợp Mg, Fe vào 285 gam dd H2SO4 đặc, nóng vừa đủ thu được khí SO2. Khí SO2 sinh ra dẫn qua dd nước vôi trong dư thu được 114 gam kết tủa.
a) Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp. b) tính nồng độ phần trăm của dd H2SO4 đã dùng và nồng độ phần trăm của các muối sinh raHãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right);n_{SO_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
0,2------------------------>0,2
\(2Fe+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,2---------------------------------------->0,3
\(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2+2H_2O\)
0,15<--------------------------------0,15
=> \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,2.56}{0,2.56+0,15.64}.100\%=53,85\%\\\%m_{Cu}=100\%-53,85\%=46,15\%\end{matrix}\right.\)

a) n Fe = a(mol) ; n Cu = b(mol)
=> 56a + 64b = 4,8(1)
n SO2 = 2,24/22,4 = 0,1(mol)
Bảo toàn e :
3n Fe + 2n Cu = 2n SO2
<=> 3a + 2b = 0,2(2)
Từ (1)(2) suy ra a = b = 0,04
%m Fe = 0,04.56/4,8 .100% = 46,67%
%m Cu = 100% -46,67% = 53,33%
b)
n KOH = 0,15
Ta có :
1 < n KOH / n SO2 = 0,15/0,1 = 1,5 < 2 nên muối sinh ra là Na2SO3(x mol) và NaHSO3(y mol)
2NaOH + SO2 $\to$ Na2SO3 + H2O
NaOH + SO2 $\to$ NaHSO3
Theo PTHH :
n SO2 = a + b = 0,1
n NaOH = 2a + b = 0,15
Suy ra a= 0,05 ; b = 0,05
m muối = 0,05.126 + 0,05.104 = 11,5 gam
Bài 2 :
- Gọi số mol Fe và Cu lần lượt là a, b mol
Ta có : mhh = mFe + mCu = 56a + 64b = 4,8
Bte : 3a + 2b = 0,2
=> a = b =0,04mol
a, Ta có : mFe =n.M = 2,24g ( 46,7% )
=> %Cu = 53,3%
b, Ta thấy sau phản ứng thu được K+, SO3-2 xmol, HSO3- y mol
BtS : x + y = 0,1
BTĐT : 2x + y = 0,15
=> x =y = 0,05 mol
=> mM = mK2SO3 + mKHSO3 = 13,9g

a/ \(n_{SO_2}=\dfrac{3,08}{22,4}=0,1375\left(mol\right);n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
2Fe + 6H2SO4(đ) ---to---> Fe2(SO4)3 + 6SO2 + 3H2O
x 3x
Cu + 2H2SO4(đ) ---to---> CuSO4 + SO2 + 2H2O
y y
Fe + 2HCl ----> FeCl2 + H2
x x
Cu + 2HCl -----> CuCl2 + H2
y y
Ta có hệ pt: \(\left\{{}\begin{matrix}3x+y=0,1375\\x+y=0,075\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,03125\left(mol\right)\\y=0,04375\left(mol\right)\end{matrix}\right.\)
\(m_{hh}=0,03125.56+0,04375.64=4,55\left(g\right)\)
\(\%m_{Fe}=\dfrac{0,03125.56.100\%}{4,55}=38,46\%\)
b, \(n_{Ba\left(OH\right)_2}=0,1.1,2=0,12\left(mol\right)\)
Ta có: \(T=\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,1375}{0,12}=1,1458\)
=> tạo ra 2 muối là BaSO3 và Ba(HSO3)2
SO2 + Ba(OH)2 ---> BaSO3 + H2O
x x x
2SO2 + Ba(OH)2 ----> Ba(HSO3)2
y 0,5y 0,5y
Ta có hệ pt: \(\left\{{}\begin{matrix}x+y=0,1375\\x+0,5y=0,12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1025\left(mol\right)\\y=0,035\left(mol\right)\end{matrix}\right.\)
\(m_{muối}=0,1025.217+0,5.0,035.299=27,475\left(g\right)\)

\(n_{CaCO3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố C: \(n_{CO}=n_{CaCO_3}=0,02\left(mol\right)\)
\(n_{Cu}=\dfrac{1,92}{64}=0,03\left(mol\right)\)
CuO + CO -------> Cu + CO2
0,02-------->0,02-->0,02
CuO + H2 -------> Cu + H2O
0,01<--------0,03-0,02=0,01
Phần trăm về thể tích cũng là phần trăm về số mol
=>\(\%V_{H_2}=\dfrac{0,01}{0,01+0,02}.100=33,33\%\)
=> %VCO=100- 33,33=66,67%
\(\%m_{H_2}=\dfrac{2.0,01}{2.0,01+44.0,02}.100=2,22\%\)
%mCO= 100-2,22=97,78%
b) \(V_{CO_2}=0,02.22,4=0,448\left(l\right)\)

Đáp án C
Đặt a, b, c là số mol của Fe3O4, Cu2S, FeS2
m(X) = 232a + 160b + 120c = 24,72 gam 1
Muối gồm: Fe3+ ( 3a+c mol); Cu2+ 2b mol) → SO42− ( 4,5a + 2b + 1,5c) mol
→ m(muối) = 56∙3a+c) + 64∙2b + 96∙4,5a + 2b+ 1,5c) = 55,6 gam 2
m(kết tủa) = 107∙3a+c) + 98∙2b + 233∙4,5a + 2b + 1,5c) = 124,86 gam 3;
Giải 1, 2, 3 → a = 0,06; b = 0,03; c = 0,05 →%(Cu2S) = 19,42%

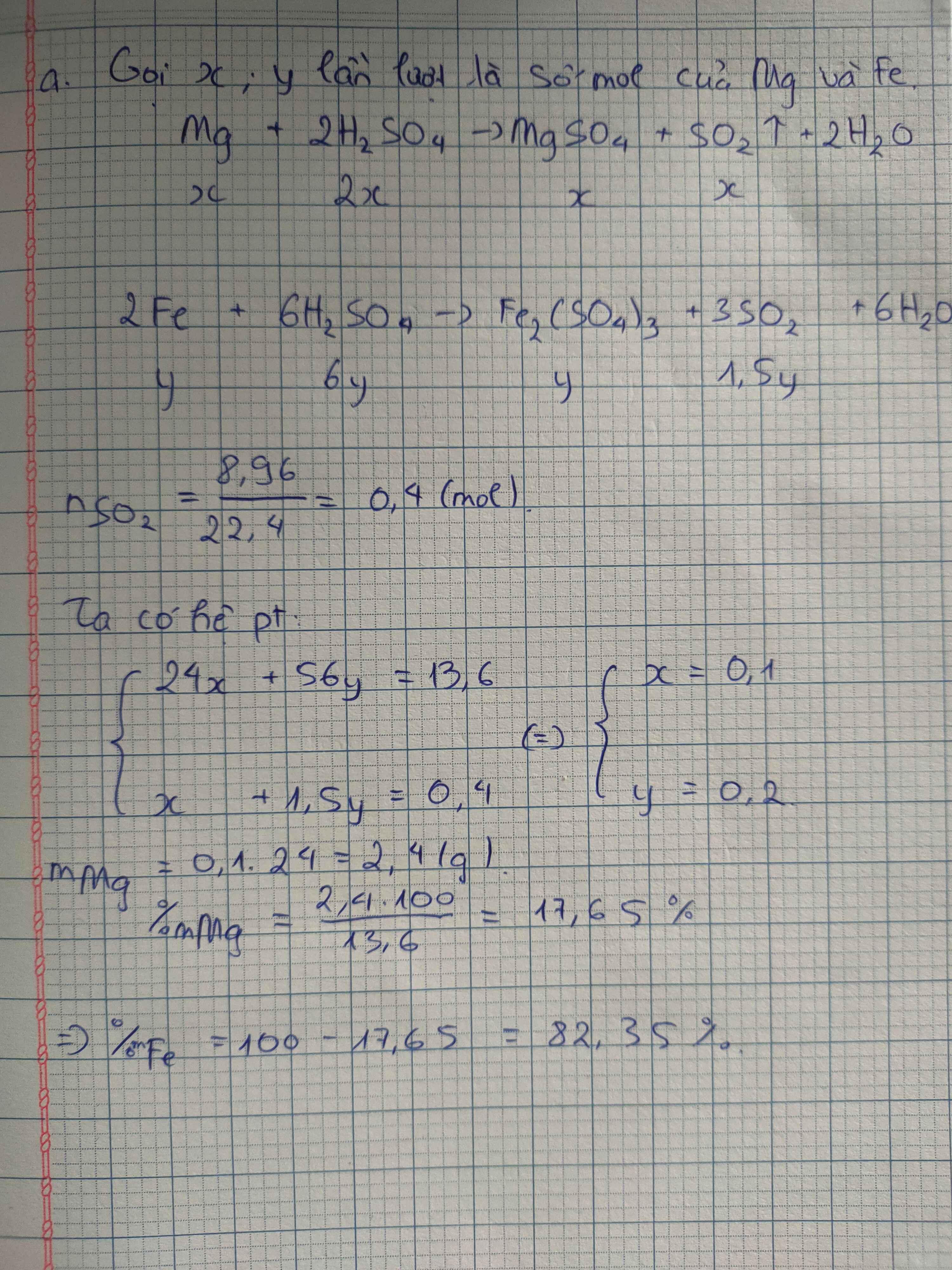

a)\(n_{CaSO_3\downarrow}=0,95\left(mol\right)\)
Bảo toàn ntố S: \(n_{SO2}=n_{CaSo_3}=0,95\left(mol\right)\)
Đặt \(\left\{{}\begin{matrix}n_{Fe}=x\\n_{Mg}=y\end{matrix}\right.\)\(\Rightarrow56x+24y=28,8\)(1)
Bảo toàn electron: \(3x+2y=2.n_{SO_2}=1,9\)
\(\Rightarrow\left\{{}\begin{matrix}56x+24y=28,8\\3x+2y=1,9\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,5\end{matrix}\right.\)
\(\Rightarrow\%Fe=\dfrac{56.0,3}{28,8}.100\%=58,3\%\)\(\Rightarrow\%Mg=41,7\%\)
b) Bảo toàn Mg: \(n_{Mg}=n_{MgSO_4}=0,5\left(mol\right)\) ; Bảo toàn Fe: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,15\left(mol\right)\)
Bảo toàn S : \(n_{H_2SO_4}=n_{MgSO_4}+3n_{Fe_2\left(SO_4\right)_3}+n_{SO_2}=1,9\left(mol\right)\)
\(\Rightarrow C\%H_2SO_4=\dfrac{1,9.98}{285}.100\%=65,3\%\)
\(m_{dd}=m_{Kl}+m_{ddH_2SO_4}-m_{SO_2}=28,8+285-0,95.64=253\left(g\right)\)
(sau p/u)
\(\Rightarrow C\%_{MgSO_4}=\dfrac{0,5.120}{253}.100\%=23,71\%\)
\(C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,15.400}{253}.100\%=23,71\%\)
cho e xin PTHH với