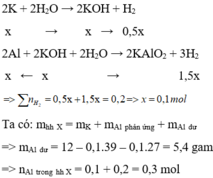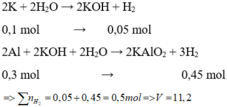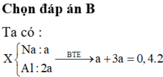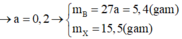Bài 1: a.Cho 26,5g hỗn hợp chất rắn X gồm CaCO3 và Na2CO3 vào dung dịch axit clohidric đến khi chất rắn tan hết thì thu được bao nhiêu lít khí (đktc)?
b. Một hỗn hợp X gồm CH3COOH và C2H5OH. Cho m gam X tác dụn với lượng dư kim loại natri thu được 5,6 lít khí (Đktc). Nếu thêm một ít dung dịch H2SO4 đặc vào m gam X và đun nóng thì thu được 17,6g CH3COOH (hiệu suất pứ đạt 80%). hãy xác định m
Bài 2: Cho vào bình kín 400ml hỗn hợp khí X (gồm một hidrocacbon và nito) và 900ml khí oxi (lấy dư so với giả thiết) rồi bật tia lửa để đốt cháy hết hidrocacbon trong X. Sau khí pứ xong thu được hỗn hợp khí Y có thể tích 1400ml. Dẫn Y lần lượt đi qua bình 1 chứa dung dịch axit sunfuric đặc, dư và bình 2 chứa dung dịch NaOH dư, thấy bình 1 hấp thụ được 60ml khí, bình 2 hấp thụ được 400 ml khí, còn lại 400ml khí ko bị hấp thụ. Các thể tích đo ở cùng điều kiện, các pứ xảy ra hoàn toàn.
a. Tính thể tích hidrocacbon trong hỗn hợp X
b. Tìm công thức hóa học của hidrocacbon trong hỗn hợp X