Tính số mol của 28 gam Fe. 10 gam CaCO
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, Xin lỗi bạn ạ, mình không biết làm :((
b, VO2 = nO2 * 22,4 = 1 * 22,4 = 22,4 (lít)
VH2 = nH2 * 22,4 = 1,5 * 22,4 = 33,6 (lít)
VCO2 = nCO2 * 22,4 = 0,4 *22,4 =8,96 (lít)
c, nFe = mFe / MFe = 28/56 = 0,5 (mol)
nHCl = mHCl / MHCl = 36,5/36,5 = 1 (mol)
nC6H12O6 = mC6H12O6 / MC6H12O6 = 18/5352 = 0,003
Đây nha bạn !! :))

+ Số mol của 28 gam Fe : \(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{28}{56}=0,5\left(mol\right)\)
+ Số mol của 28 gam Nitơ: \(n_{N2}=\frac{m_{N2}}{M_{N2}}=\frac{28}{28}=1\left(mol\right)\)

a) \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
b) \(n_{Al}=\dfrac{13,5}{27}=0,5\left(mol\right)\)
c) \(n_{CO_2}=\dfrac{11}{44}=0,25\left(mol\right)\)
d) \(m_{O_2}=\dfrac{4,958.0,99}{0,082.\left(273+25\right)}=0,2\left(mol\right)\)
e) \(m_{CH_4}=\dfrac{12,359.0,99}{0,082\left(273+25\right)}=0,5\left(mol\right)\)
a: \(n=\dfrac{28}{56}=0.5\left(mol\right)\)
b: \(n=\dfrac{13.5}{27}=0.5\left(mol\right)\)

a) nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{5,6}{56}=0,1\left(mol\right)\)
nCu=\(\frac{m_{Cu}}{M_{Cu}}=\frac{64}{64}=1\left(mol\right)\)
nAl= \(\frac{m_{Al}}{M_{Al}}=\frac{27}{27}=1\left(mol\right)\)
b) \(n_{CO_2}=\frac{m_{CO_2}}{M_{CO_2}}=\frac{44}{44}=1\left(mol\right)\)
\(n_{H_2}=\frac{m_{H_2}}{M_{H_2}}=\frac{4}{2}=2\left(mol\right)\)
a) nFe = 5,6/56 = 0,1 mol
nCu = 64/64 = 1 mol
nAl = 27/27 = 1 mol
b) nCO2 = 44/44 = 1 mol
=> VCO2 = 1.22,4 = 22,4 l
nH2 = 4/2 = 2 mol
=> VH2 = 2.22,4 = 44,8 l

a/ nCaO = 11,2 : 56 = 02 mol
ptpư ; CaCO3 -----> CaO + CO2
1mol 1mol 1mol
x mol? 0,2 mol
thep ptpư ta thấy số mol CaCO3 cần dùng là
0,2x 1 : 1 = 0,2 mol
b/ câu b câu hỏi giống a tương tự Đáp số 0.125 mol
c/ theo ptpư trên thì nCaCO3 = nCO2
=> nCO2 = 3.5 mol => VCO2=3.5x22,4=78.4l
d/ ta có nCO2 = 13.44/22.4 =0.6 mol
ptpư : nCaCO3 = nCaO= n CO2 = 0.6
=> mCaCO3 = 0.6x100 = 60g ( tham gia )
mCaO = 0.6x56 =33.6 (tạo thành )

Đáp án B
Sử dụng công thức n = m/M
Số mol C bằng 4,8/12 = 0,4 mol
Số mol O 2 bằng 16/32 = 0,5 mol
Số mol Fe bằng 0,56/56 = 0,01 mol.
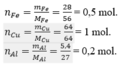
Ta có:
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{28}{56}=0,5\left(mol\right)\)
\(n_{CaO}=\dfrac{m_{CaO}}{M_{CaO}}=\dfrac{10}{56}\approx0,2\left(mol\right)\)
Vậy...
Số mol của Fe:
\(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right)\)
Số mol của CaCO:
\(n_{CaCO}=\dfrac{10}{68}=0,1\left(mol\right)\)