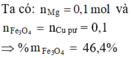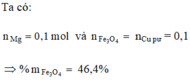Cho 10,8 g hỗn hợp A gồm Mg và Cu vào dung dịch H2 SO4 loãng dư sau phản ứng người ta thu được 8,96 lít khí H2 ở điều kiện tính chất và 3 gam chất rắn không tan a) Tính thành phần trăm của hỗn hợp A theo khối lượng b) cho hỗn hợp a vào dung dịch KOH dư.Tính thể tích khí H2 sinh ra ở điều kiện tính chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
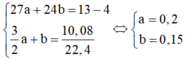
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.

Bài 6 : Chất rắn không tan là Cu
$m_{Cu} = 6,4(gam)$
Gọi $n_{Al} = a(mol) ; n_{Mg} = b(mol) \Rightarrow 27a + 24b + 6,4 = 14,2(1)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 +3 H_2$
$Mg + H_2SO_4 \to MgSO_4 + H_2$
$n_{H_2} = 1,5a + b = 0,4(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,1
$\%m_{Al} = \dfrac{0,2.27}{14,2}.100\% = 38,03\%$
$\%m_{Mg} = \dfrac{0,1.24}{14,2}.100\% =16,9\%$
$\%m_{Cu} = 100\% -38,03\% - 16,9\% = 45,07\%$
Bài 7 :
Gọi $n_{CuO} = a(mol) ; n_{ZnO} = b(mol) \Rightarrow 80a + 81b = 12,1(1)$
$CuO + 2HCl \to CuCl_2 + H_2O$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
$n_{HCl} = 2a + 2b = 0,1.3 = 0,3(2)$
Từ (1)(2) suy ra a= 0,05 ; b = 0,1
$\%m_{CuO} = \dfrac{0,05.80}{12,1}.100\% = 33,06\%$
$\%m_{ZnO} = 100\% - 33,06\% = 66,94\%$

m(rắn)=mCu=6,4(g)
nH2=6,72/22,4=0,3(mol)
PTHH: Mg + H2SO4 -> MgSO4+ H2
nMg=nH2=0,3(mol)
=>a=m(hhCu,Mg)=mCu+mMg=6,4+0,3.24= 13,6(g)
=>a=13,6(g)
Chúc em học tốt!