Bài 16. Hòa tan hoàn toàn 12,8 gam đồng bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc).Phương trình hóa học như sau: Cu + H2SO4 đặc,nóng CuSO4 + SO2 + H2Oa.Lập PTHH theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, QT oxi hóa, QT khử. b.Tính V.Bài 17: Hòa tan hoàn toàn 11,2 gam sắt bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc). Phương trình phản...
Đọc tiếp
Bài 16. Hòa tan hoàn toàn 12,8 gam đồng bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc).Phương trình hóa học như sau: Cu + H2SO4 đặc,nóng CuSO4 + SO2 + H2O
a.Lập PTHH theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, QT oxi hóa, QT khử. b.Tính V.
Bài 17: Hòa tan hoàn toàn 11,2 gam sắt bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc). Phương trình phản ứng như sau: Fe + H2SO4 đặc,nóng Fe2(SO4)3 + SO2 + H2O a.Lập PTHH theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, QT oxi hóa, QT khử. b.Tính V
. Bài 18: Hoà tan hoàn toàn 8,8 gam hỗn hợp A gồm Cu và Fe trong 100ml dd H2SO4 x (mol/lít) theo các phản ứng sau: Fe + H2SO4 đặc,nóng Fe2(SO4)3 + SO2 + H2O (1) Cu + H2SO4 đặc,nóng CuSO4 + SO2 + H2O (2) Sau khi các phản ứng kết thúc thu được dung dịch B và 4,48 lít khí SO2 (đktc). a.Lập các phương trình hóa học (1) và (2). b.Tính % khối lượng mỗi chất có trong A. c.Để tác dụng vừa hết với các chất có trong dung dịch B cần 200ml dung dịch NaOH 4M. Tính giá trị của x
. Bài 19: Hoà tan hết 17 gam hỗn hợp bột A gồm Al và FeCO3 trong 300ml dung dịch HCl 2M thu được dung dịch B và 5,6 lít hỗn hợp khí C (đktc). a) Tính % khối lượng mỗi chất có trong A. b) Tính thể tích dung dịch NaOH 0,5M cần để trung hoà hết lượng axit có trong dung dịch B
. Bài 20: Hoà tan hết 13 gam hỗn hợp bột A gồm Mg và Na2CO3 trong Vml dung dịch H2SO4 1M (loãng) thu được 4,48 lít hỗn hợp khí B (đktc) và dung dịch C. a) Tính % khối lượng mỗi chất có trong A. b) Cho dung dịch C tác dụng với dung dịch Ba(OH)2 dư, lọc kết tủa nung đến khối lượng không đổi được 62,25 gam chất rắn. Tính V.



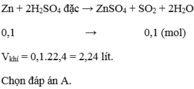
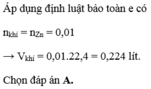


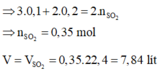

\(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4đặc,nóng}\rightarrow CuSO_4+SO_2+2H_2O|\)
1 2 1 1 1
0,1 0,1
\(n_{SO2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
Chúc bạn học tốt
Cu + 2H2SO4\(\rightarrow\)CuSO4 + 2H2O +SO2
0,1 \(\rightarrow\) 0,1
nCu= \(\dfrac{6,4}{64}\)=0,1 mol
vSO2= 0,1 . 22,4= 22 4 ( lit)