Lấy 93,9 gam Fe3O4 trộn với Al được hỗn hợp X. Nung hỗn hợp trong mỗi trường không có không khí, sau khi phản ứng xảy ra hoàn toàn, ta thu được hỗn hợp Y. Chia Y thành 2 phần:
- Phần 1: tác dụng với dung dịch NaOH dư cho 0,672 lít khí H2
- Phần 2: tác dụng với dung dịch HCl dư cho 18,816 lít khí H2
Tính khối lượng các chất trong hỗn hợp ban đầu

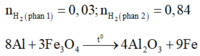


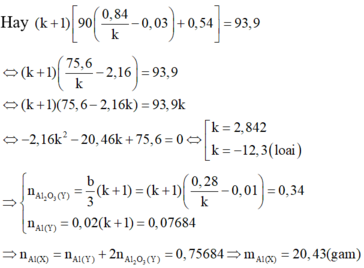
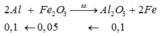

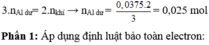

\(3Fe_3O_4\left(0,75a\right)+8Al\left(2a\right)\rightarrow9Fe\left(2,25a\right)+4Al_2O_3\left(a\right)\)
Cho hỗn hợp sau tác dụng với dung dịch NaOH có khí thoát ra => Al dư sau pứ
Đặt nAl2O3 = a (mol); nAl dư = b(mol)
Chia Y làm 2 phần bằng nhau:
Phần 1:Cho tác dụng với dung dịch NaOH:
\(2Al\left(0,02\right)\rightarrow3H_2\left(0,03\right)\)
\(\Rightarrow0,5b=0,02\left(I\right)\)
Phần 2: Cho tác dụng với dung dịch HCl dư: nH2 = 0,84 (mol)
\(Fe\left(1,125a\right)\rightarrow H_2\left(1,125a\right)\)
\(2Al\left(0,5b\right)\rightarrow3H_2\left(0,75b\right)\)
\(\Rightarrow1,125a+0,75b=0,84\left(II\right)\)
Từ (I) và (II) => a = 0,72 mol; b = 0,04 mol
=> nAl ban đầu = 2a + b = 1,48(mol)
=> mAl = 39,96 gam => mFe3O4 = 53,94 gam
PTHH:
\(8Al+3Fe_3O_4\rightarrow4Al_2O_3+9Fe\)
\(2Al\left(0,02\right)+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\left(0,03\right)\)
\(Fe\left(nx\right)+2HCl\rightarrow FeCl_2+H_2\left(nx\right)\)
\(2Al\left(0,02n\right)+6HCl\rightarrow2AlCl_3+3H_2\left(0,03n\right)\)
\(\left\{{}\begin{matrix}n_{H_2\left(1\right)}=\dfrac{0,672}{22,4}=0,03\\n_{H_2\left(2\right)}=\dfrac{18,816}{22,4}=0,84\end{matrix}\right.\)
Vì cho vào NaOH có khí thoát ra chứng tỏ Al dư.
Gọi số mol của \(Fe,Al_2O_3,Al\) trong phần 1 là: \(\left\{{}\begin{matrix}Fe:x\\Al_2O_3:\dfrac{4x}{9}\\Al:0,02\end{matrix}\right.\) và phần 2 là: \(\left\{{}\begin{matrix}Fe:nx\\Al_2O_3:\dfrac{4nx}{9}\\Al:0,02n\end{matrix}\right.\)
Ta có: \(nx+0,03n=0,84\left(1\right)\)
Số mol của \(Fe,Al_2O_3,Al\)có trong Y là: \(\left\{{}\begin{matrix}Fe:x\left(n+1\right)\\Al_2O_3:\dfrac{4x}{9}\left(n+1\right)\\Al:0,02\left(n+1\right)\end{matrix}\right.\)
Khối lượng của Y là:
\(56x\left(n+1\right)+\dfrac{102.4x\left(n+1\right)}{9}+27.0,02\left(n+1\right)=93,9\)
\(\Leftrightarrow15200nx+15200x+81n-14004=0\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}nx+0,03n=0,84\\15200nx+15200x+81n-14004=0\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,18\\n=4\end{matrix}\right.\)(còn 1 bộ nghiệm nữa mà nó âm nên mình loại luôn rồi nhé).
\(\Rightarrow n_{Al}=\dfrac{2.4.0,18}{9}.\left(4+1\right)+0,02.\left(4+1\right)=0,9\left(mol\right)\)
\(\Rightarrow m_{Al}=0,9.27=24,3\left(g\right)\)
\(\Rightarrow m_{Fe_3O_4}=93,9-24,3=69,6\left(g\right)\)