Cho 9,2 gam Na vào 200g dung dịch chứ Fe2(SO4)3 4% và Al2(SO4)3 6,84%. Sau phản ứng, người ta tách kết tủa ra và nung đến khối lượng không đổi. Tính khối lượng chất rắn thu được sau khi nung
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Ta có: nNa = \(\dfrac{9,2}{23}\)=0,4 mol
nFe2(SO4)3 = 0,125.0,16 = 0,02 mol.
nAl2(SO4)3 = 0,15.0,16 = 0,04 mol.
PTHH:
Na + H2O ---> NaOH + \(\dfrac{1}{2}\) H2.
0,4...................0,4
6NaOH + Fe2(SO4)3 ---> 3Na2SO4 + 2Fe(OH)3
0,12<---------0,02---------------------------->0,04
6NaOH + Al2(SO4)3 ---> 3Na2SO4 + 2Al(OH)3
0,24 <------0,04---------------------------->0,08
=> NaOHdư= 0,4 - 0,12 - 0,24 = 0,04 mol.
NaOH + Al(OH)3 --> NaAlO2 + 2 H2O
0,04------->0,04
=> Kết tủa gồm: Fe(OH)3 0,04 mol và Al(OH)3 0,08 - 0,04 = 0,04 mol
=> Chất rắn là Fe2O3 : 0,02 mol và Al2O3 0,02 mol
=> mrắn = 0,02.160 + 0,02.102 = 5,24g
b) Muối thu được : NaAlO2 và Na2SO4
nNaAlO2 = 0,04mol
nNa2SO4 = 0,02.3+0,04.3 =0,18 mol.
mdd sau pứ =\(9,2+200-2.0,2-107.0,04-78.0,04=201,4\left(g\right)\)
\(C\%_{Na_2SO_4}=\dfrac{142.0,18}{201,4}.100=12,71\%\)
\(C\%_{NaAlO_2}=\dfrac{82.0,04}{201,4}.100=1,63\%\)

\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\) (1)
\(6NaOH+Fe_2\left(SO_4\right)_3\rightarrow2Fe\left(OH\right)_3+3Na_2SO_4\) (2)
\(n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right);n_{Fe_2\left(SO_4\right)_3}=\dfrac{200.4\%}{400}=0,04\left(mol\right)\)
\(TheoPT\left(1\right):n_{NaOH}=n_{Na}=0,4\left(mol\right)\)
Lập tỉ lệ PT (2) : \(\dfrac{0,4}{6}>\dfrac{0,04}{1}\)
=> Sau phản ứng NaOH dư
\(2Fe\left(OH\right)_3-^{t^o}\rightarrow Fe_2O_3+3H_2O\)
Bảo toàn nguyên tố Fe: \(n_{Fe_2O_3}.2=n_{Fe_2\left(SO_4\right)_3}.2\Rightarrow n_{Fe_2O_3}=0,04\left(mol\right)\)
=> \(m_{Fe_2O_3}=0,04.160=6,4\left(g\right)\)
Dung dịch A: \(Na_2SO_4:0,12\left(mol\right);NaOH_{dư}:0,4-0,24=0,16\left(mol\right)\)
\(m_{ddsaupu}=9,2+200-0,08.107=200,64\left(g\right)\)
\(C\%_{Na_2SO_4}=\dfrac{0,12.142}{200,64}=8,5\%\)
\(C\%_{NaOH}=\dfrac{0,16.40}{200,64}.100=3,2\%\)
@Thảo Phương
Chị ơi chỗ \(C\%_{Na_2SO_4}=\dfrac{0,12.142}{200,64}=8,5\%\) thiếu nhấn vs \(100\%\) (nhưng kết quả vẫn đúng)

PTHH: 2Na + 2H2O -> 2NaOH+H2
Ta có:
nNa = 9,2/23 = 0,4 mol = nNaOH
=> mFe2(SO4)3 = 200.4% = 8 gam
=> nFe2(SO4)3 = 8/(56.2 + 96.3 )= 0,02 mol;
=> mAl2(SO4)3 = 6,84%.200 = 13,68 gam
=> nAl2(SO4)3 = 13,68/(27.2 + 96.3) = 0,04 mol
PTHH: Fe2(SO4)3 + 6NaOH -> 2Fe(OH)3 + 3Na2(SO4)3
Ta có:
nFe(OH)3 = 2nFe2(SO4)3 = 0,04 mol;
nNaOH còn lại = 0,2 − 0,02.6 = 0,08 mol
Al2(SO4)3 + 6NaOH -> 2Al(OH)3 + 3Na2SO4
nNaOH < 6nAl2(SO4)3 => nAl(OH)3 = 13nNaOH = 0,08/3
Nung kết tủa:
2Fe(OH)3 \(\underrightarrow{^{t^o}}\) Fe2O3 + 3H2O
2Al(OH)3 \(\underrightarrow{^{t^o}}\) Al2O3 + 3H2O
=> nFe2O3 = 1/2nFe(OH)3 = 0,02 mol
=> nAl2O3 = 1/2nAl(OH)3 = 0,04/3
=> mrắn = 0,02.160 + 0,04/3.(27.2 + 16.3) = 4,56 gam

n Fe2(SO4)3 = 0,02 mol ; n Al2(SO4)3 = 0,04 mol
Chất rắn chắc chắn có Fe2O3 , có thể có Al2O3
=> n Fe2O3 = n Fe2(SO4)3 = 0,02 mol
=> nAl2O3 = 0,02 mol => n Al(OH)3 = 0,04 mol < n Al3+ .
Xét 2 TH:
+/ TH1: tạo kết tủa , kết tủa không tan
=> n NaOH = 3n Al(OH)3 + 6nFe3+ = 0,24 mol = n Na
=> a = 5,52g .Không có đáp án => Loại
+/TH2: kết tủa tan 1 phần:
=> n Al(OH)3 = 4nAl3+ - n NaOH => n NaOH = 0,28 mol
=> tổng số mol NaOH phản ứng là : 0,28 + 0,02.2.3 = 0,4 mol
=>a =9,2g
=>B

\(n_{NaOH}=0,4mol\)
\(n_{Fe_2\left(SO_4\right)_3}=0,16.0,125=0,02mol\)
\(n_{Al_2\left(SO_4\right)_3}=0,16.0,25=0,04mol\)
Fe2(SO4)3+6NaOH\(\rightarrow\)2Fe(OH)3+3Na2SO4
0,02
Al2(SO4)3+6NaOH\(\rightarrow\)2Al(OH)3+3Na2SO4
0,04
Số mol NaOH(Pu)=6(0,02+0,04)=0,36mol
Số mol NaOH(dư)=0,4-0,36=0,04mol
Số mol Al(OH)3=0,04.2=0,08mol
Al(OH)3+NaOH\(\rightarrow\)NaAlO2+2H2O
Dựa vào tỉ lệ mol ta thấy Al(OH)3 còn dư=0,08-0,04=0,04mol
2Al(OH)3\(\rightarrow\)Al2O3+3H2O
Số mol Al2O3=0,04:2=0,02mol
2Fe(OH)3\(\rightarrow\)Fe2O3+3H2O
Số mol Fe2O3=0,02mol
mChất rắn=0,02(102+160)=5,24g
phương trình của NaOH và Al2(SO4)3 theo mình là sai
8NaOH + Al2(SO4)3  2NaAlO2 + 3Na2SO4 + 4H2O
2NaAlO2 + 3Na2SO4 + 4H2O

Nhận thấy 3 < nOH- : nAl3+ = 1,4 : 0,4 < 4 → xảy ra quá trình hòa tan kết tủa
Al3+ + 3OH- → Al(OH)3↓
x------3x
Al3+ + 4OH- → Al(OH)4-
y-------4y
Ba2+ + SO42- → BaSO4↓
0,7-----0,6------->0,6
Ta có hệ 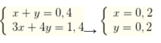
Vậy kết tủa gồm nAl(OH)3 = 0,2 mol, nBaSO4 = 0,6 mol
Nung kết tủa đến khối lượng không đổi: Al2O3: 0,1 mol và nBaSO4 = 0,6 mol → mchất rắn = 150 gam.
Đáp án A
