Hòa tan hết 0,54 gam Al trong 70ml dd HCl 1M thu được dd X . Cho 75 ml dd NaOH 1M vào X sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa . Gía trị của m là :
A. 1,56 B. 1,17 C. 0,39 D. 0,78
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
nAl = 0,02 mol; nCl– = 0,07 mol; nNa+ = 0,075 mol.
Ghép NaCl
⇒ còn dư (0,075 – 0,07 = 0,005) mol Na+
⇒ ghép với AlO2– tạo NaAlO2.
||⇒ ghép được 0,005 mol NaAlO2 và còn dư (0,02 – 0,005 = 0,015) mol nguyên tố Al.
► Dùng nguyên tố đó ghép vào ↓ ⇒ nAl(OH)3 = 0,015 mol
⇒ m = 1,17(g)

Giải thích:
nAl = 0,02 mol
nHCl = 0,07 mol
nNaOH = 0,075 mol
Al + 3HCl → AlCl3 + 1,5H2
Bđ: 0,02 0,07
Pư: 0,02 0,06 0,02
Sau: 0 0,01 0,02
Vậy dung dịch X gồm: Al3+ (0,02 mol) và H+ dư (0,01 mol)
Khi cho 0,075 mol NaOH vào dd X:
H+ + OH- → H2O
0,01 0,01
Al3+ + 3OH- → Al(OH)3
0,02 0,06 0,02
Al(OH)3 + OH- → AlO2- + 2H2O
0,005←0,005
Vậy khối lượng Al(OH)3: m = (0,02-0,005).78 = 1,17 gam
Đáp án B

Đáp án B
nAl = 0,02 mol
nHCl = 0,07 mol
nNaOH = 0,075 mol
Al + 3HCl → AlCl3 + 1,5H2
Bđ: 0,02 0,07
Pư: 0,02 0,06 0,02
Sau: 0 0,01 0,02
Vậy dung dịch X gồm: Al3+ (0,02 mol) và H+ dư (0,01 mol)
Khi cho 0,075 mol NaOH vào dd X:
H+ + OH- → H2O
0,01 0,01
Al3+ + 3OH- → Al(OH)3
0,02 0,06 0,02
Al(OH)3 + OH- → AlO2- + 2H2O
0,005←0,005
Vậy khối lượng Al(OH)3:
m = (0,02-0,005).78 = 1,17 gam

Chọn B
nAl = 0,02 mol
nHCl = 0,07 mol
nNaOH = 0,075 mol
Al + 3HCl → AlCl3 + 1,5H2
Bđ: 0,02 0,07
Pư: 0,02 0,06 0,02
Sau: 0 0,01 0,02
Vậy dung dịch X gồm: Al3+ (0,02 mol) và H+ dư (0,01 mol)
Khi cho 0,075 mol NaOH vào dd X:
H+ + OH- → H2O
0,01 0,01
Al3+ + 3OH- → Al(OH)3
0,02 0,06 0,02
Al(OH)3 + OH- → AlO2- + 2H2O
0,005←0,005
Vậy khối lượng Al(OH)3: m = (0,02-0,005).78 = 1,17 gam

Đáp án B
nAl = 0,02 mol
nHCl = 0,07 mol
nNaOH = 0,075 mol
Al + 3HCl → AlCl3 + 1,5H2
Bđ: 0,02 0,07
Pư: 0,02 0,06 0,02
Sau: 0 0,01 0,02
Vậy dung dịch X gồm: Al3+ (0,02 mol) và H+ dư (0,01 mol)
Khi cho 0,075 mol NaOH vào dd X:
H+ + OH- → H2O
0,01 0,01
Al3+ + 3OH- → Al(OH)3
0,02 0,06 0,02
Al(OH)3 + OH- → AlO2- + 2H2O
0,005←0,005
Vậy khối lượng Al(OH)3: m = (0,02-0,005).78 = 1,17 gam


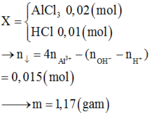
Câu A.1,56
pthh: 2Al + 6HCl -> 2AlCl3 + 3H2
0,02 0,07
nAl = 0,54/27= 0,02(mol)
nHCl= 0,07.1= 0,07(mol)
==> nAlCl3= 0,02(mol)
pthh: 3NaOH + AlCl3 ---> 3NaOH + Al(OH)3(kết tủa)
-> nAlCl3= 0,02 mol
-> mAlcl3= 0,02.78= 1,56
Đáp án B mới đúng
\(n_{Al}=\dfrac{0,54}{27}=0,02mol\)
nHCl=0,07.1=0,07mol
nNaOH=0,075.1=0,075 mol
2Al+6HCl\(\rightarrow\)2AlCl3+3H2
Tỉ lệ:\(\dfrac{0,02}{2}< \dfrac{0,07}{6}\)\(\rightarrow\)HCl dư
nHCl(pu)=3nAl=0,02.3=0,06 mol
nHCl(dư)=0,07-0,06=0,01 mol
\(n_{AlCl_3}=n_{Al}=0,02mol\)\(\rightarrow\)X(AlCl3 0,02 mol, HCl 0,01 mol)
HCl+NaOH\(\rightarrow\)NaCl+H2O
nNaOH(pu)=nHCl=0,01 mol
nNaOH(còn)=0,075-0,01=0,065mol
AlCl3+3NaOH\(\rightarrow\)Al(OH)3+3NaCl
\(n_{NaOH}=3n_{AlCl_3}=3.0,02=0,06mol\)
nNaOH dư=0,065-0,06=0,005 mol
\(n_{Al\left(OH\right)_3}=n_{AlCl_3}=0,02mol\)
Al(OH)3+NaOH\(\rightarrow\)NaAlO2+2H2O
Dựa vào tỉ lệ mol và số mol ta thấy :
\(n_{Al\left(OH\right)_3\left(pu\right)}=n_{NaOH}=0,005mol\)
\(n_{Al\left(OH\right)_3\left(dư\right)}=0,02-0,005=0,015mol\)
m=(27+17.3).0,015=1,17 gam