Hỗn hợp Cu, Fe, Al nặng 10,15g được hòa atan bằng HNO3 đặc thoát ra 2,24 dm3 khí NO2 (đktc). Nếu hòa tan hh bằng dd HCl dư tì thoát ra 3,92 dm3 khí H2(đktc) . Viết pt phản ứng và tính % khối lượng mỗi KL.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi x, y ,z là số mol Cu, Fe, Al.
=> 64x + 56y + 27z = 10.15 (1)
Khi cho vào HNO3 đặc nguội thì chỉ có Cu phản ứng
Cu + 4HNO3 --------> Cu(NO3)2 + 2NO2 + 2H2O
x--------------------------------------...
=> 2x = nNO2 = 2.24/22.4 = 0.1 (2)
Khi cho vào HCl thì có Cu không phản ứng
Fe + 2HCl ----------> FeCl2 + H2
y--------------------------------------...
2Al + 6HCl ----------> 2AlCl3 + 3H2
z--------------------------------------...
=> y+3z/2 = nH2 = 3.92/22.4=0.175 (3)
Giải (1), (2), (3) => x=0.05, y=0.1, z=0.05
mCu = 0.05*64=3.2 gam
mFe = 0.1*56=5.6gam
mAl = 0.05*27=1.35 gam
%mCu = 3.2*100/10.15=31.5
%mFe = 5.6*100/10.15=55.2
%mAl = 1.35*100/10.15=13.3.
Source: Yahoo.
Trần Hữu Tuyển giúp mình với, mình giải hệ rồi nhưng kết quả sai

\(PTHH:\text{Cu+4HNO3}\rightarrow\text{Cu(NO3)2+2NO2+2H2O}\)
\(\text{Fe+2HCl}\rightarrow\text{FeCl2+H2}\)
\(\text{2Al+6HCl}\rightarrow\text{2AlCl3+3H2}\)
Gọi a, b lần lượt là số mol của Fe và Al
Ta có :
\(\left\{{}\begin{matrix}\text{nNO2=0,1(mol)}\\\text{nH2=0,175(mol)}\end{matrix}\right.\)
=>nCu=0,05(mol)
=>mCu=0,05x64=3,2(g)
\(\Rightarrow\left\{{}\begin{matrix}\text{56a+27b=6,95}\\\text{a+3b/2=0,175}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\text{a=0,1}\\\text{b=0,05}\end{matrix}\right.\)
\(\text{%Cu=3,2/10,15x100=31,53%}\)
\(\text{%Fe=0,1x56/10,15x100=55,17%}\)
\(\text{%Al=13,3%}\)
Cu + 4HNO3 -----> Cu(NO3)2 + 2NO2 + 2H2O
Fe+2HCl---->FeCl2+H2
2Al+6HCl---->2AlCl3+3H2
n\(_{NO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Theo pthh1
n\(_{Cu}=\frac{1}{2}n_{NO2}=0,05\left(mol\right)\)
%m Cu=\(\frac{0,05.64}{10,15}.100\%=31,53\%\)
m\(_{Fe}+m_{Al}=10,15-3,2=6,95\left(g\right)\)
n\(_{H2}=\frac{3,92}{22,4}=0,175\left(mol\right)\)
Gọi n\(_{Fe}=x,n_{Al}=y\)
Theo bài ra ta có pt
\(\)\(\left\{{}\begin{matrix}56x+27y=6,95\\x+1,5x=0,175\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
%m\(_{Fe}=\frac{0,1.56}{10,15}.100\%=55,17\text{%}\)
% m Al=100-55,17-31,53=13,3%

Đặt \(\left\{{}\begin{matrix}n_{Al}=x\\n_{Zn}=y\\n_{Cu}=z\end{matrix}\right.\) ( mol )
\(m_{hh}=27x+65y+64z=22,8\left(g\right)\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
x 1,5x ( mol )
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
y y ( mol )
\(n_{H_2}=1,5x+y=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) (2)
B là Cu
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
z z ( mol )
\(n_{CuO}=z=\dfrac{5,5}{80}=0,06875\left(mol\right)\) (3)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\\z=0,06875\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Zn}=0,2.65=13\left(g\right)\\m_{Cu}=22,8-5,4-13=4,4\left(g\right)\end{matrix}\right.\)

a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_{Zn}\) \(\Rightarrow m_{Zn}=0,1\cdot65=6,5\left(g\right)\)
\(\Rightarrow\%m_{Zn}=\dfrac{6,5}{10}\cdot100\%=65\%\) \(\Rightarrow\%m_{Cu}=35\%\)
c) Theo PTHH: \(n_{HCl}=2n_{Zn}=0,2mol\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,2\cdot36,5}{5\%}=146\left(g\right)\)

Khi cho hỗn hợp Al, Fe, Zn vào dung dịch NaOH dư thì chỉ có Zn và Al tham gia phản ứng tạo H2(0,225 mol), phần chất rắn không tan là Fe
Cho Fe phản ứng với lượng dư HCl tạo ra 0,1 mol khí → nFe = nH2 = 0,1 mol → mAl + mZn= 16,7- 5,6 = 11,1
Gọi số mol của Al và Zn lần lượt là x, y
Ta có hệ 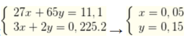
→ %Al = 0 , 05 . 27 16 , 7 ×100% = 8,08 %.
Đáp án D

2Al+6HCl---->2AlCl3+3H2
Al2o3+6HCl--->2AlCl3+3H2O
Cu+HCl--> không p/u
2Cu + O2---->2CuO
ncuO=2,75/80=0.034375(mol)
Cứ 2 mol Cu---à 2 mol CuO
0.034375<------0.034375
mCu=0,034375.64=2,2(g)
--->%mCu=2,2.100/10=22%
nH2=3,36/22,4=0,15(mol)
cứ 2 mol Al----->3 mol H2
0.1<-----0.15
mAl :0,1.27=2.7(g)
--->%mAl=2,7.100/10=27%
---->%mAl2o3=100%-27%-22%=51%

cu ko tac dung voi HCl=>2,75g la khoi luong cua Cu => %Cu = 2,75/10*100=27,5%
n H2 = 3,36/22,4= 0,15 mol
pt 2Al + 6HCl -----> 2AlCl3 + 3H2
=> n Al = 2/3n H2 = 2/3 *0,15= 0,1 mol => m Al = 0,1 *27 = 2,7g
=> % Al = 2,7/10*100= 27%
=> %Al2O3 = 100%-27,5%-27%=45,5%

Nếu số lít SO2 =12.32 thì số mol sẽ là 0.55 nên Kl Cu =35.2(g).Không phù hợp yêu cầu của đề bài.

Tính số mol " NO2 ; HNO3 ; H2
đặt n,Cu,Al,Fe lần lượt là x,y,z
=> ...
lập hệ
tự giải nhé !
nHNO3 tính kiểu gì