tính ph của dung dịch tạo thành sau khi trộn 200ml dung dịch a gồm h2so4 0,1m, hcl ,02m và 300ml gồm ba(oh)2 0.15m naoh 0.1m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
nOH-= 0,03 mol; nBa2+ = 0,01 mol
nH+ = 0,035 mol; nSO4(2-) = 0,015 mol
H+ + OH- → H2O
0,035 0,03
nH+ dư = 5.10-3 mol; [H+] dư = 5.10-3/0,5 = 0,01 suy ra pH = 2

Đáp án C
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13

Đáp án B
nH+ = 0,1 .2.0,05 + 0,1.0,1 =0,02
nOH- = 0,1.0,2 + 0,1.0,1.2 = 0,04
⇒ Trong dung dịch sau phản ứng có nOH- dư = 0,04 – 0,02 = 0,02 mol
V dd thu = 100 + 100 = 200ml
⇒ [OH-] = 0,1 ⇒ pH = 13
Đáp án B.

H+ + OH- ® H2O
Tổng số mol OH-: (0,1.2 + 0,1).0,1 = 0,03 mol
Tổng số mol H+ : (0,0375.2 + 0,0125).0,4 = 0,035 mol
Số mol H+ dư: 0,035 – 0,03 = 0,005 mol ® [H+]= 0,01M ® pH = 2
Ví dụ 2. Cho dung dịch A là một hỗn hợp: H2SO4 2.10-4M và HCl 6.10-4M Cho dung dịch B là một hỗn hợp: NaOH 3.10-4M và Ca(OH)2 3,5.10-4M
a) Tính pH của dung dịch A và dung dịch B
b) Trộn 300ml dung dịch A với 200ml dung dịch B được dung dịch C. Tính pH của dung dịch C.

Đáp án B
nOH- = 0,1.2.0,1 + 0,1.0,1 = 0,03
nH+ = 0,4.2.0,0375 + 0,4.0,0125 = 0,035
⇒ Trong X có H+ dư
⇒ nH+/X =0,035 – 0,03 = 0,005; VX = 100 + 400 = 500ml
⇒ [H+] = 0,01 ⇒ pH = 2.
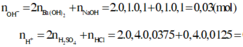
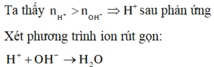
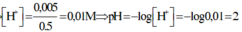

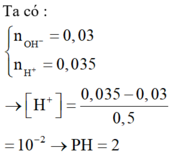
Có:nH2SO4 =0,02(mol) ; nHCl=0,04(mol)
=>nH(+)=0,08(mol)
Có: nBa(OH)2 =0,045 (mol); nNaOH=0,03(mol)
=>nOH(-)=0,12(mol)
H(+) +OH(-) ------>H2O
0,008-----0,008
=>nOH(-) dư=0,04(mol)
[OH(-) dư]=0,04/0,5=0,08(M)
=>pH= -log(0,08) =1,1