Câu 1 : Khử hoàn toàn 8g oxit sắt bằng CO . Dẫn toàn bộ lượng khí sinh ra bình đựng nước vôi trong thấy khối lượng tăng m(g) . Chất rắn thu được sau phản ứng khử cho tác dụng với HCl dư thu đk 2,24(l) H2 ( đktc) .
a. Xác định CTHH của oxit.
b. Tìm m .
Câu 2: Ngâm 1 lá Cu trong 400ml đ AgNO3 ( D =1.05g/mol) đến khi khi phản ứng kết thúc thấy Cu tăng 7.6 g
a. Tính nồng độ mol của dd AgNO3 đã dùng.
b. Tính C% các chất sau phản ứng.






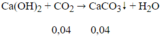

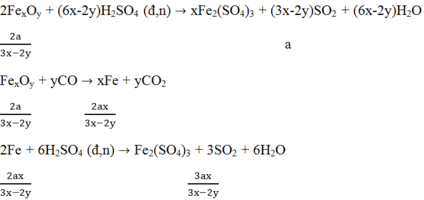
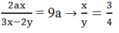
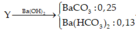
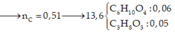
Câu 1: Đặt CÔng thức FexOy
FexOy+yCO\(\rightarrow\)xFe+yCO2
CO2 bị Ca(OH)2 hấp thụ nên m=\(m_{CO_2}\)
Fe+2HCl\(\rightarrow\)FeCl2+H2
\(n_{Fe}=n_{H_2}=0,1mol\)
Theo PTHH 1 ta có: noxit\(=\dfrac{1}{x}.n_{Fe}=\dfrac{0,1}{x}mol\)
MOxit\(=\dfrac{m}{n}=\dfrac{8}{\dfrac{0,1}{x}}=80x\)
Hay 56x+16y=80x suy ra 24x=16y hay 3x=2y\(\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Fe2O3
\(n_{CO_2}=\dfrac{y}{x}n_{Fe}=\dfrac{3}{2}.0,1=0,15mol\)
m=0,15.44=6,6g
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
-Gọi số mol Cu là x theo PTHH số mol Ag là 2x
- Độ tăng khối lượng=108.2x-64x=7,6
152x=7,6 hay x=0,05mol
\(n_{AgNO_3}=2n_{Cu}=2.0,05=0,1mol\)
\(m_{AgNO_3}=0,1.170=17g\)
\(m_{AgNO_3}=0,1.170=17g\)
\(m_{ddAgNO_3}=v.D=400.1,05=420g\)
\(C\%=\dfrac{17.100}{420}\approx4,05\%\)
mdd=420-7,6=412,4g
\(n_{Cu\left(NO_3\right)_2}=n_{Cu}=0,05mol\)
\(m_{Cu\left(NO_3\right)_2}=0,05.188=9,4g\)
\(C\%=\dfrac{9,4.100}{412,4}\approx2,3\%\)