Cho 250 ml dung dịch NaOH 4M vào 50 ml dung dịch Al2(SO4)3 2M. Thu được dung dịch X. tính khối lượng kết tủa sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) \(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
PTHH: \(Al_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,03<----------------------0,01
=> nNaOH min = 0,03 (mol)
=> \(C_{M\left(NaOH\right)}=\dfrac{0,03}{0,2}=0,15M\)
2) \(n_{Al_2O_3}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0,3.0,25=0,075\left(mol\right)\)
PTHH: \(6NaOH+Al_2\left(SO_4\right)_3\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,45<------0,075-------------------------->0,15
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
0,05<----0,05
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
0,1<-------0,05
=> nNaOH max = 0,5 (mol)
=> \(V_{dd}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
3)
\(n_{KOH\left(1\right)}=0,15.1,2=0,18\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(1\right)}=\dfrac{4,68}{78}=0,06\left(mol\right)\)
\(n_{AlCl_3}=0,1.x\left(mol\right)\)
Do khi cho KOH tác dụng với dd Y xuất hiện kết tủa
=> Trong Y chứa AlCl3 dư
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
0,18---->0,06----------------->0,06
\(n_{KOH\left(2\right)}=0,175.1,2=0,21\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(2\right)}=\dfrac{2,34}{78}=0,03\left(mol\right)\)
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
(0,3x-0,18)<--(0,1x-0,06)------->(0,1x-0,06)
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
(0,1x-0,09)<-(0,1x-0,09)
=> \(\left(0,3x-0,18\right)+\left(0,1x-0,09\right)=0,21\)
=> x = 1,2

Đáp án B
6NH3+ Al2(SO4)3+ 6H2O→ 2Al(OH)3+3 (NH4)2SO4 (1)
NaOH + Al(OH)3 → NaAlO2+ H2O (2)
Có nAl(OH)3= nNaOH= 0,01.2= 0,02 mol
→ nAl2(SO4)3= 1 2 . nAl(OH)3= 0,01 mol
→ CM Al2(SO4)3= 0,01/ 0,02= 0,5M

Chọn D.
nBa(OH)2 đầu = 0.15 => nOH- = 0.3
nAl2(SO4)3 = 0.25x => nAl3+ = 0.5x và nSO4(2-) = 0.75x
Khi cho 150ml Ba(OH)2 vào dd thu được 42.75g kết tủa
Thêm tiếp 200ml
=> m kết tủa theo lí thuyết = 350*42.75/150 = 99.75g > 94.2375g
=> Lúc đầu chưa tạo kết tủa cực đại, Al2(SO4)3 dư ; sau khi thêm Ba(OH)2 vào thì pứ tạo kết tủa
lớn nhất và sau đó Ba(OH)2 dư sẽ hòa tan thêm một phần kết tủa
+ Khi chưa thêm: (tính theo nBa(OH)2)
Ba2+ + SO42- ---> BaSO4
0.15 0.15 0.15
Al3+ + 3OH- ----> Al(OH)3
0.1 0.3 0.1
+ Khi thêm Ba(OH)2 vào: (tính theo nAl2(SO4)3)
Ba2+ + SO42- ---> BaSO4
0.75x-0.15 0.75x-0.15
Al3+ + 3OH- ---> Al(OH)3
0.5x-0.1 1.5x-0.3 0.5x-0.1
OH- dư + Al(OH)3 --->AlO2- + 2 H2O
0.4-1.5x+0.3 0.7-1.5x
Ta có:
m kết tủa lúc sau = m kết tủa ban đầu + mBaSO4 sau + mAl(OH)3 chưa tan lúc sau = 42.75 + 233*(0.75x-0.15) +
78*(0.5x-0.1-0.7+1.5x)
=> 330.75x - 54.6 = 94.2375
=> x = 0.45

Chọn đáp án C
Chú ý :
(1). Trong bài toán này người ta không vớt kết tủa lần đầu ra mà cứ để yên rồi đổ thêm Ba(OH)2 vào.
(2). Để mò ra đáp án nhanh bài toán này các bạn cần tư duy nhanh xem lượng kết tủa ở lần 1 và 2 có bị tan phần nào không.Điều này khá đơn giản.
+Nhìn nhanh qua đáp án cũng khẳng định được ở lần 1 muối sunfat có dư.
+Khi đổ thêm Ba(OH)2 dễ thấy Al(OH)3 bị tan vì khi x = 0,45 vẫn bị tan
Khi đó ta có
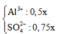
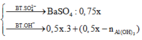
![]()
![]()
Vậy
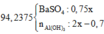
![]()
![]()
Bài này các bạn cũng có thể dùng thủ đoạn truyền thống “thử đáp án”

Chọn đáp án C
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
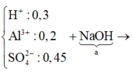
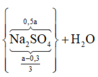
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

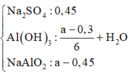
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
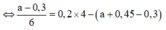
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C
\(n_{NaOH}=0,25.4=1\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=2.0,05=0,1\left(mol\right)\\ PTHH:6NaOH+Al_2\left(SO_4\right)_3\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ Vì:\dfrac{1}{6}>\dfrac{0,1}{1}\\ \Rightarrow NaOHdư\\ \rightarrow n_{Al\left(OH\right)_3}=2.0,1=0,2\left(mol\right)\\ m_{kt}=m_{Al\left(OH\right)_3}=78.0,2=15,6\left(g\right)\)
\(n_{NaOH}=0.25\cdot4=1\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0.05\cdot2=0.1\left(mol\right)\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
Lập tỉ lệ :
\(\dfrac{0.1}{1}< \dfrac{1}{6}\) \(\Rightarrow NaOHdư\)
\(n_{NaOH\left(dư\right)}=1-0.6=0.4\left(mol\right)\)
\(n_{Al\left(OH\right)_3}=0.1\cdot2=0.2\left(mol\right)\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
\(n_{NaOH}>n_{Al\left(OH\right)_3}\)
=> Kết tủa tan hoàn toàn
\(m_{\downarrow}=0\)