cho 5.94 gam kim loại R tác dụng hết với dung dịch HCl thì thu được 7.392 lít khí H2 ( đktc).
a, xác định R
b, tính khối lượng HCl đã phản ứng
c, muốn điều chế 1344 cm3 khí khí H2 ( đktc) thì cần dùng bao nhiêu gam R
biết phản ứng xảy ra theo sơ đồ
R + HCl --------> RCl3 + khí H2

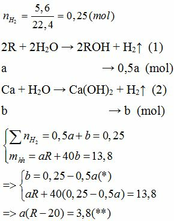
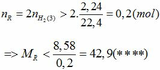
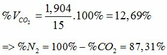
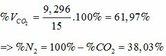
\(n_{H_2}=0,33\left(mol\right)\)
Gọi n là hóa trị của R
\(2R+2nHCl\left(0,66\right)\rightarrow2RCl_n+nH_2\left(0,33\right)\)
Ta có: \(n.n_R=2.n_{H_2}\)
\(\Leftrightarrow n.\dfrac{5,94}{R}=2.0,33\)
\(\Leftrightarrow R=9n\)
+ Với n = 1 => R = 9 (loại)
+ Với n = 2 => R = 18 (loại)
+ Với n = 3 => R = 27 (loại)
Vậy R là Nhôm (Al)
Theo PTHH: \(n_{HCl}=2n_{H_2}=0,66\left(mol\right)\)
\(\Rightarrow m_{HCl}=24,09\left(g\right)\)
c) \(n_{H_2}\left(đktc\right)=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
\(2Al\left(0,04\right)+6HCl\rightarrow2AlCl_3+3H_2\left(0,06\right)\)
Theo PTHH: \(n_{Al}=0,04\left(mol\right)\Rightarrow m_{Al}=1,08\left(g\right)\)