Đốt cháy hoàn toàn 15g hỗn hợp gồm CH4 và CO trong không khí thì thu được 16,8 lít CO2 (đktc).
a, Tính % về thể tích các khí trong hỗn hợp ban đầu.
b, Tính thể tích không khí cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + H_2O\\ 2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O\\ b) n_{CH_4} = a(mol) ; n_{C_2H_2} = b(mol)\\ \Rightarrow a + b = \dfrac{6,72}{22,4} = 0,3(1)\\ n_{O_2} = 2a + \dfrac{5}{2}b = \dfrac{22,4}{32} = 0,7(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,2\\ \%V_{CH_4} = \dfrac{0,1.22,4}{6,72}.100\% = 33,33\%\\ \%V_{C_2H_2} = 100\% - 33,33\% = 66,67\%\)
a, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(1\right)\)
Ta có: \(n_{O_2}=\dfrac{22,4}{32}=0,7\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=2x+\dfrac{5}{2}y\left(mol\right)\)
\(\Rightarrow2x+\dfrac{5}{2}y=0,7\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,3}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Đáp án B
Theo giả thiết, bảo toàn nguyên tố C và bảo toàn electron, ta có :
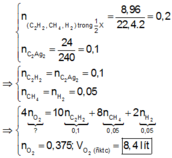

Chọn B.
Theo đề ta có: n O 2 = 1 , 225 ; n C O 2 = 1 , 05 v à n H 2 O = 1 , 05 => X no, đơn chức, mạch hở (vì n C O 2 = n H 2 O )
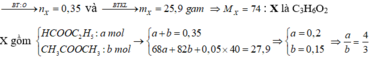

CH4+2O2-to>CO2+2H2O
x---------2x-------x
C2H4+3O2-to>2CO2+2H2O
y-------------3y------2y
=>Ta có :
\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\)
=>x=0,01, y=0,03 mol
=>%VCH4=\(\dfrac{0,01.22,4}{0,896}100\)=25%
=>%VC2H4=75%
=>m CO2=(0,01+0,03.2).44=3,08g
a, ta có PTHH :
CH4 + 2O2 \(\Rightarrow\) CO2 + 2H2O (*)
C2H4 + 3O2 \(\Rightarrow\) 2CO2 + 2H2O(+)
b, Gọi x, y lần lượ là số mol của CH4 , C2H4 ( x, y > 0 )
Ta có : nh = \(\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(\Rightarrow x+y=0,04\left(mol\right)\) (1)
lại có no2 pứ = \(\dfrac{3,52}{32}=0,11\left(mol\right)\)
\(\Rightarrow2x+3y=0,11\left(mol\right)\) (2)
Từ (1) và (2) ta có hệ pt:\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
%VCH4 = \(\dfrac{0,01}{0,04}\times100\%=25\%\)
%VC2H4 = \(\dfrac{0,03}{0,04}\times100\%=75\%\)
c, Theo pt nCO2(*) = nCH4 = 0,01 (mol)
nCO2(+) = 2nC2H4 = 0,6 (mol)
\(\Rightarrow m_{co_2}=\left(0,01+0,6\right)\times44=26,84\left(g\right)\)
CH4 + 2O2 \(\rightarrow\)CO2 + 2H2O (1)
2CO + O2 \(\rightarrow\)2CO2 (2)
nCO2=\(\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
Đặt nCH4=a
nCO=b
Ta có:
\(\left\{{}\begin{matrix}16a+28b=15\\a+b=0,75\end{matrix}\right.\)
a=0,5;b=0,25
mCH4=0,5.16=8(g)
% CH4 =\(\dfrac{8}{15}.100\%=53,3\%\)
% CO=100-53,3=46,7%
b;
Theo PTHH 1 và 2 ta có:
\(\sum n_{O_2}=0,5.2+0,25.\dfrac{1}{2}=1,125\left(mol\right)\)
VO2=1,125.22,4=25,2(lít)