X là hỗn hợp Mg và Zn, Y là dung dịch H2SO4 chưa rõ nồng độ.
- Thí nghiệm 1: Cho 24,3 gam X vào 2 lít Y được 8,96 lít H2 (đktc).
- Thí nghiệm 2: Cho 24,3 gam X vào 3 lít Y được 11,2 lít H2 (đktc).
Tính nồng độ mol của dung dịch Y và khối lượng Mg, Zn có trong hỗn hợp.

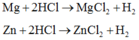
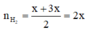
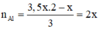
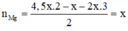
PTHH:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Thí nghiệm 1:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,4}{2}=0,2M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,4\left(mol\right)\left(1\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(2\right)\)
Giải hệ hai phương trình (1) và (2) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,04\left(mol\right)\\n_{Zn}=0,36\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,96\left(g\right)\\n_{Zn}=23,4\left(g\right)\end{matrix}\right.\)
Thí nghiệm 2:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,5}{2}=0,25M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,5\left(mol\right)\left(3\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(4\right)\)
Giải hệ hai phương trình (3) và (4) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Zn}=0,3\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=4,8\left(g\right)\\n_{Zn}=19,5\left(g\right)\end{matrix}\right.\)
vì sao CM và khối lượng lại ra 2 kết quả vậy ạ?