Tính khối lượng AlNO3 kết tinh khỏi dung dịch khi làm lạnh 450g dung dịch bão hòa ở 80oC xuống 20oC (Biết độ tan của AlNO3 Ở 80oC là 668g và ở 20oC LÀ 222g)?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2
160 gam dung dịch CuSO4 chứa mCuSO4=160.10%=16 gam
-> nCuSO4=16/160=0,1 mol
-> mH2O=160-16=144 gam -> nH2O\(=\dfrac{144}{18}\)=8 mol
-> số mol các nguyên tử trong dung dịch=8.3+0,1.6=24,6 mol
-> Sau khi cô cạn số mol các chất =\(\dfrac{24,6}{2}\)=12,3 gam
-> nH2O thoát ra =\(\dfrac{12,3}{3}\)=4,1 mol -> mH2O=4,1.18=73,8 gam

Câu 2:
1.
\(m_{H_2O}=\dfrac{600}{100+50}.100=400\left(g\right)\\ m_{CuSO_4\left(kết.tinh\right)}=\dfrac{400}{100}.\left(50-15\right)=140\left(g\right)\\ n_{CuSO_4.5H_2O}=n_{CuSO_4}=\dfrac{140}{160}=0,875\left(mol\right)\\ m_{CuSO_4.5H_2O\left(kết.tinh\right)}=0,875.250=218,75\left(g\right)\)
2,
Số nguyên tử bằng một nửa ban đầu => số mol giảm đi một nửa
\(m_{CuSO_4}=160.10\%=16\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\\ m_{H_2O}=160-16=144\left(g\right)\Rightarrow n_{H_2O}=\dfrac{144}{18}=8\left(mol\right)\\ \Rightarrow n_{H_2O\left(bay.hơi\right)}=\dfrac{1}{2}.\left(0,1+8\right)=4,05\left(mol\right)\\ \Rightarrow m_{H_2O\left(bay.hơi\right)}=4,05.18=72,9\left(g\right)\)

n CuO = 64/80 = 0,8(mol)
CuO + H2SO4 → CuSO4 + H2O
0,8..........0,8............0,8.................(mol)
m dd H2SO4 = 0,8.98/20% = 392 gam
=> mdd sau pư = m CuO + mdd H2SO4 = 64 + 392 = 456 gam
Gọi n CuSO4.5H2O = a(mol)
CuSO4 + 5H2O → CuSO4.5H2O
a................5a...................a............(mol)
Sau khi tách tinh thể:
n CuSO4 = 0,8 - a(mol)
m dd = m dd sau pư - m CuSO4.5H2O = 456 - 250a(gam)
Suy ra :
C% = S/(S + 100).100%
<=> 160(0,8 - a)/(456 -250a) = 25/(25+100)
<=>a = 0,3345
=> m CuSO4.5H2O = 0,3345.250 = 83,625 gam

Chọn B
Độ tan của R 2 S O 4 ở 80 o C là 28,3 gam
→ Trong 1026,4 gam dung dịch có
m R 2 S O 4 = 1026,4.28,3 100 + 28,3 = 226,4 g

Vậy kim loại R là Na.

mdd = 86,26 – 60,26 = 26(g)
mct = 66,26 – 60,26 = 6 (g) ⇒ mH2O = 26 - 6 = 20g
Độ tan của muối ở 20°C là:
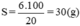
Vậy độ tan của muối ở 20°C là 30 gam

Ở 700C:
48.1 gam AlCl3 tan tối đa trong 100 gam nước tạo thành 148.1 gam dung dịch.
a gam AlCl3 tan tối đa trong b gam nước tạo thành 500 gam dung dịch
\(\Rightarrow a=\dfrac{500\cdot48.1}{148.1}=162.3\left(g\right)\)
\(b=337.7\left(g\right)\)
- Ở 20oC,
44.9 gam AlCl3 tan tối đa trong 100 gam nước tạo thành 144.9 g dung dịch.
c gam AlCl3 tan tối đa trong 337.7 g nước tạo thành dung dịch.
\(\Rightarrow c=\dfrac{337.7\cdot44.9}{100}=151.6\left(g\right)\)
\(m_{AlCl_3\left(kt\right)}=a-c=162.3-151.6=10.7\left(g\right)\)

\(m_{Na_2CO_3\left(20^oC\right)}=243.\dfrac{21,5}{100+21,5}=43\left(g\right)\)
\(\Rightarrow m_{H_2O}=243-43=200\left(g\right)\)
Cứ 100g nước ở 90oC hoà tan được 43,9g Na2CO3
=> 200g nước _________________ 87,8g Na2CO3
\(\Rightarrow m_{Na_2CO_3\left(thêm.vào\right)}=87,8-43=44,8\left(g\right)\)

Trong 100g H2O ở 800C hòa tan 668g AlNO3 ở 200C hòa tan 222g AlNO3
\(\Rightarrow\)Ở 800C khi hạ nhiệt độ xuống 200C thì 768g dung dịch tách ra 446g AlNO3.
Vậy trong 450g dung dịch tách ra x(g) AlNO3.
=>\(x=\dfrac{450\cdot446}{768}\approx261,33\left(g\right)\)