a. Hãy tính cách pha chế 50g dung dịch CuSO4 có nồng độ 10%.
b. Hãy tính cách pha chế 50ml dung dịch CuSO4 có nồng độ 1M.
c. Từ dung dịch HNO3 5M có sẵn hãy trình bày cách pha chế 150ml dung dịch HNO3 0,25M .
d. Tu dung dịch MgSO4 2M làm thế nào pha chế được 100ml dung dịch MgSO4 0,4M.

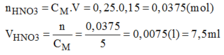
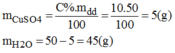
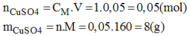
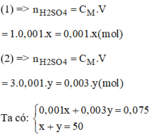
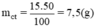
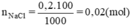
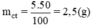
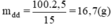
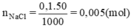
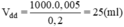
a) Tính toán
\(\dfrac{m_{ct}}{m_{dd}}.100\%=10\%\)
\(\dfrac{m_{CuSO_4}}{50}.100\%=10\%\)
\(\Rightarrow m_{CuSO_4}=10:100.50=5\left(g\right)\)
Khối lượng CuSO4 cần dùng là 5g.
Cách pha chế: Hướng dẫn SGK
Câu b) Tương tự với nồng độ mol