Bài 5: Cho 400 ml dung dịch E gồm AlCl3 x mol/lít và Al2(SO4)3 y mol/lít tác dụng với 612 ml dung dịch
NaOH 1M, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 (dư) thì thu được 33,552 gam kết tủa. Tìm x,y.

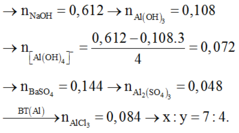

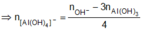
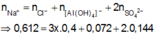
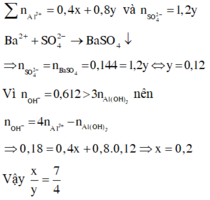




400 ml dd E gồm AlCl3 xM và Al2(SO4)3 yM + 0,612 mol NaOH → 0,108 mol Al(OH)3.
400 ml E + BaCl2 dư → 0,144 mol ↓BaSO4.
=> n BaSO4 = 3y = 0,144 → y = 0,048 (*).
Ở TN1:
nAl(OH)3 = nAl3+ - (nOH- - 3nAl3+)
= 4nAl3+ - nOH-
= 4(x + 2y) - 0,612 = 0,108 (**)
Từ (*), (**) => x = 0,084.