cho 8,4(g) bột sắt tác dụng với 2,24(g) khí oxi(đktc) tạo thành oxit sắt từ.tính khối lượng oxit sắt từ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


3Fe+2O2-to>Fe3O4
Áp dụng định luật bảo toàn khối lượng :
mFe+mO2=mFe3O4
=>mFe3O4=4,2+1,6=5,8g
mgfe + mgo2 = fe3o4
4,2g +1,6g = fe3o4
5,8g =fe3o4
vậy khối lg sắt từ tạo ra là 5,8g

a,3Fe +2O2→to→Fe3O4
b,CT:m=n.M
c, Số mol Fe là: nFe=8,4/56=0,15 mol
Theo pt:nFe3O4=nFe=0,15 mol
Khối lượng Fe3O4: mFe3O4=n.M=0,15.232=34,8
d,Số mol O2 pư là:nO2=2/3 . 0,15=0,1 mol
Khối lượng O2 phản ứng là:m=0,1.32=3,2 g
khối lượng kk cần dùng là: 3,2:21%=15,238g

\(a,3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ n_{Fe}=\dfrac{16,8}{56}=0,3\left(kmol\right)\\ n_{O_2}=\dfrac{2}{3}.0,3=0,2\left(kmol\right)\\ V_{O_2\left(\text{đ}ktc\right)}=0,2.1000.22,4=4480\left(l\right)\\ n_{Fe_3O_4}=\dfrac{1}{3}.0.3=0,1\left(kmol\right)\\ m_{Fe_3O_4}=232.0,1=23,2\left(kg\right)\)

3Fe+2O2-to>Fe3O4
0,03-----0,02---------0,01
n Fe=\(\dfrac{1,68}{56}\)=0,03 mol
n O2=\(\dfrac{1,6}{32}\)=0,05 mol
=>O2 dư
=>m Fe3O4=0,01.232=23,2g
=>m O2 dư=0,03.32=0,96g

Đáp án A
Ta có sơ đồ phản ứng:
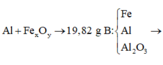
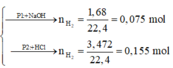
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
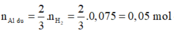
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
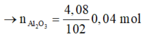
Ta có:
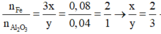
=> Oxit sắt cần tìm là Fe2O3

\(n_{Zn}=\dfrac{3,25}{65}=0,05mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,05 0,1 0,05 ( mol )
\(V_{H_2}=0,05.22,4=1,12l\)
\(m_{HCl}=0,1.36,5=3,65g\)
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
0,05 0,0375 ( mol )
\(m_{Fe}=0,0375.56=2,1g\)

\(m_{tăng}=m_O=1.39-1=0.39\left(g\right)\)
\(CT:Fe_xO_y\)
\(\)\(n_{Fe}=\dfrac{1}{56}\simeq0.02\left(mol\right)\)
\(n_O=\dfrac{0.39}{16}\simeq0.02\left(mol\right)\)
\(x:y=n_{Fe}:n_O=0.02:0.02=1:1\)
\(CT:FeO\)
Đề: Cho 1(g) bột sắt tiếp xúc với oxi một thời gian thấy khối lượng bột sắt đã vượt lên 1,39(g). Nếu chỉ tạo thành 1 oxit duy nhất thì đó có thể là oxit nào?
Trả lời:
m tăng= mO= 1,39-1= 0,39g
nO= 0,39/16= 0,02 mol
nFe= 1/56= 0,02 mol
nFe: nO= 0.02:0,02= 1:1 nên oxit sắt là FeO


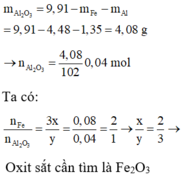
nFe=8.4/56=0.15(mol)
nO2=2.24/22.4=0.1(mol) ( đề bài chắc ghi sai 2.24lít thành 2.24gam nhỉ)
PTHH:
3Fe + 2O2 -->(nhiệt độ) Fe3O4
B/đ`:0.15 0.1 0 (mol)
P/ứ: 0.15-->0.1--> 0.05(mol)
SauP/ứ:0 0 0.05 (mol)
=> sau phả ứng thu được 0.05 mol Fe3O4
=>mFe3O4=0.05*232=11.69g)
Ta có: \(n_{Fe}=\frac{8,4}{56}=0,15\left(mol\right)\\ n_{O_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 3Fe + 2O2 -to-> Fe3O4
Theo các PTHH và đề bài, ta có:
\(\frac{0,15}{3}=\frac{0,1}{2}\)
=> Không có chất nào dư nên ta tính theo chất nào cũng được.
=> \(n_{Fe_3O_4}=\frac{0,1}{2}=0,05\left(mol\right)\\ =>m_{Fe_3O_4}=232.0,05=11,6\left(g\right)\)