cho tui hỏi : 1 quặng sắt chứa 90% Fe3O4 còn lại là tạp chất , nếu dùng khí hidro dể khử 0,5 tấn quặng thì số lượng sắt thu được là bao nhiêu?hi zúp cái nhi tui ko hiểu dạng này .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Khối lượng Fe3O4 trong 0,5 tấn quặng sắt là :
\(90\%.0,5=0,45\left(tons\right)=450000\left(g\right)\)
=> \(n_{Fe_3O_4}=\frac{m}{M}=\frac{56250}{29}\left(mol\right)\)
PTHH : \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
Theo PTHH : \(n_{Fe}=\frac{168750}{29}\left(mol\right)\)
=> \(m_{Fe}=325862,069\left(g\right)\approx0,326\left(tons\right)\)

\(0,58\left(tấn\right)=580000\left(g\right)\\ \Rightarrow m_{Fe_3O_4}=580000\cdot80\%=464000\left(g\right)\\ \Rightarrow n_{Fe_3O_4}=\dfrac{464000}{232}=2000\left(mol\right)\\ PTHH:Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\\ \Rightarrow n_{Fe}=3n_{Fe_3O_4}=8000\left(mol\right)\\ \Rightarrow m_{Fe}=8000\cdot56=336000\left(g\right)=0,336\left(tấn\right)\)

Chọn A

=> khối lượng F e 3 O 4 có trong quặng là 0,552 (tấn)
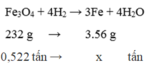
Vậy m F e = ( 0 , 522 . 3 . 56 ) : 232 = 0 , 378 t ấ n .

Khối lượng của Fe3O4 trong quặng là: 0,5 * 90% = 0,45 tấn
PTHH: 4H2 + Fe3O4 →3 Fe + 4H2O
...................+ 232 g........3*56 g.................
Vậy khử 450 g Fe3O4 thì đc x g Fe
⇒ x = \(\dfrac{450\cdot3\cdot56}{232}\) = 325,9 g = 0,326 tấn
Vậy....

\(m_{Ca_3\left(PO_4\right)_2}=20\cdot40\%=8\left(tấn\right)=8000\left(kg\right)\)
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{8000}{310}=\dfrac{800}{31}\left(kmol\right)\)
Bảo toàn nguyên tố P :
\(n_{P_2O_5}=n_{Ca_3\left(PO_4\right)_2}=\dfrac{800}{31}\left(kmol\right)\)
\(m_{P_2O_5}=\dfrac{800}{31}\cdot142=3664.5\left(kg\right)\)



0,5 tấn = 500000g
mFe3O4có trong 0,5 tấn quặng= \(\frac{50000\cdot90}{100}\)=450000g
\(\Rightarrow\)nFe3O4= \(\frac{450000}{232}\)=\(\frac{56250}{29}\)mol
PTHH: Fe3O4 + 4H2 \(\rightarrow\) 3Fe + 4H2O
Theo pthh, nFe=\(\frac{168750}{29}\)mol
\(\Rightarrow\)mFe= \(\frac{168750}{29}\)*56 =325862,069g
vậy lượng Sắt thu được là 325862,069g