Trộn 35,2g Cu với hỗn hợp CaCO3 và MgCO3 đc 53,6g hỗn hợp A. Nung nóng hỗn hợp ngoài không khí đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng hỗn hợp ko đổi . Tính khối lượng của CaCO3 và MgCO3 trong hỗn hợp đầu.
P/s: ai bik trl giúp e vs ạ!!!



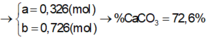
PTHH:
2Cu + O2 =(nhiệt)=> 2CuO
0,55----------------------0,55
CaCO3 =(nhiệt)=> CaO + CO2
a-------------------------a
MgCO3 =(nhiệt)=> MgO + CO2
b-------------------------b
Ta có: nCu = \(\frac{35,2}{64}=0,55\left(mol\right)\)
Đặt số mol CaCO3 , MgCO3 trong hỗn hợp A lần lượt là a, b (mol)
Theo đề ra, ta có:mA = mCu + mCaCO3 + mMgCO3 = 53,6
\(\Leftrightarrow m_{CaCO3}+m_{MgCO3}=53,6-m_{Cu}\)
\(\Leftrightarrow100a+84b=53,6-35,2=18,4\left(1\right)\)
Mặt khác: Sau khi nung khối lượng chất rắn không đổi
Suy ra: mCuO + mCaO + mMgO = 53,6
\(\Leftrightarrow0,55\times80+56a+40b=53,6\)
\(\Leftrightarrow56a+40b=53,6-0,55\times80=9,6\left(2\right)\)
Từ (1), (2), ta có hệ phương trình: \(\left\{\begin{matrix}56a+40b=9,6\\100a+84b=18,4\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{\begin{matrix}m_{CaCO3}=0,1\times100=10\left(gam\right)\\m_{MgCO3}=0,1\times84=8,4\left(gam\right)\end{matrix}\right.\)
\(2Cu\left(0,55\right)+O_2\left(0,275\right)\rightarrow2CuO\left(0,275\right)\)
\(CaCO_3\left(x\right)\rightarrow CaO\left(x\right)+CO_2\left(x\right)\)
\(MgCO_3\left(y\right)\rightarrow MgO\left(y\right)+CO_2\left(y\right)\)
\(n_{Cu}=\frac{35,2}{64}=0,55\)
Gọi số mol của CaCO3 và MgCO3 lần lược là x, y ta có
\(100x+84y=53,6\left(1\right)\)
Khối lượng O2 thêm vào đúng bằng khối lượng CO2 thoát ra nên
\(44\left(x+y\right)=0,275.32\Leftrightarrow x+y=0,2\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{\begin{matrix}100x+84y=53,6\\x+y=0,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=2,3\\y=-2,1\end{matrix}\right.\)
Đề sai hay sao thế