Cho 200ml dd A gồm Nacl 2M và KNO3 1M vào 100 ml dung dịch B gồm Naoh 2M ,Kcl 1.5M thu được dung dịch C.a)Tính nồng độ ion C. b)Cô cạn dung dịch C thu được m(g) muối khan.Tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
$n_{BaCl_2} = 0,1 < n_{H_2SO_4} = 0,2$ nên $H_2SO_4$ dư
$n_{BaSO_4} = n_{BaCl_2} = 0,1(mol)$
$m_{BaSO_4} = 0,1.233 = 23,3(gam)$
b)
A gồm :
$HCl : 0,1.2 = 0,2(mol)$
$H_2SO_4\ dư : 0,2 - 0,1 = 0,1(mol)$
$V_{dd} = 0,1 + 0,1= 0,2(lít)$
$C_{M_{HCl}} = \dfrac{0,2}{0,2} = 1M$
$C_{M_{H_2SO_4}} = \dfrac{0,1}{0,2} = 0,5M$
c)
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{NaOH} = 2n_{H_2SO_4\ dư} = 0,2(mol)$
$m_{dd\ NaOH} = \dfrac{0,2.40}{15\%} = 53,33(gam)$

a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)

Đáp án A
Từ nhỗn hợp khí và tỉ khối hơi
⇒ nN2O = 0,01 và nNO = 0,03.
nNaOH trung hòa = nHNO3 dư = 0,04 mol
⇒ Sơ đồ tóm tắt ta có:

PT theo m hỗn hợp:
24a + 232b = 9,6 (1)
PT bảo toàn e:
2a + b – 8c = 0,01×8 + 0,03×3 = 0,17 (2)
PT theo ∑nHNO3:
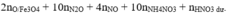
Û 8b + 10c = 0,34 (3)
+ Giải hệ ta có:
a = 0,11 || b = 0,03 || c = 0,01.
⇒ Sau trung hòa dung dịch chứa

⇒ mMuối = 42,26 gam


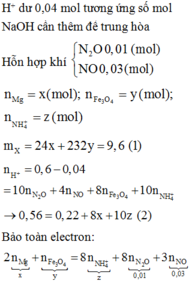
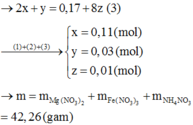
$n_{Na^+} = 0,2.2 + 0,1.2 = 0,6(mol)$
$n_{Cl^-} = 0,2.2 + 0,1.1,5 = 0,55(mol)$
$n_{NO_3^-} = 0,2.1 = 0,2(mol)$
$n_{OH^-} = 0,1.2 = 0,2(mol)$
$n_{K^+} = 0,2.1 + 0,1.1,5 = 0,35(mol)$
$V_{dd} = 0,2 + 0,1 = 0,3(lít)$
Suy ra:
$[Na^+] = \dfrac{0,6}{0,3} = 2M$
$[Cl^-] = \dfrac{0,55}{0,3}= 1,83M$
$[OH^-] = [NO_3^-] = \dfrac{0,2}{0,3} = 0,67M$
$[K^+] = \dfrac{0,35}{0,3} = 1,167M$
$m_{muối} = m_{NaCl} + m_{KNO_3} + m_{KCl} = 0,2.2.58,5 + 0,2.101 + 0,1.1,5.74,5$
$= 54,775(gam)$