Một chất có ứng dụng rộng rãi ở các vùng quê,có thành phần % về khối lượng các nguyên tố K,Al,S lần lượt là 8,228 % , 5,696 % , 13,502 % còn lại là oxi và hiđro.Xác định công thức của chất đó.Biết trong chất đó S có số oxi hóa cao nhất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)

Gọi công thức chung là FexSyOz
%O2=48%
x:y:z=\(\dfrac{28}{56}:\dfrac{24}{32}:\dfrac{48}{16}=0,5:0,75:3=2:3:12\)
=> CTHH Fe2(SO4)3
tên: Sắt (III)sunfat

Trong 1 mol hợp chất:
$n_H=\dfrac{98.2,04\%}{1}\approx 2(mol)$
$n_S=\dfrac{98.32,65\%}{32}\approx 1(mol)$
$n_O=\dfrac{98-2-32}{16}=4(mol)$
$\to CTHH:H_2SO_4$
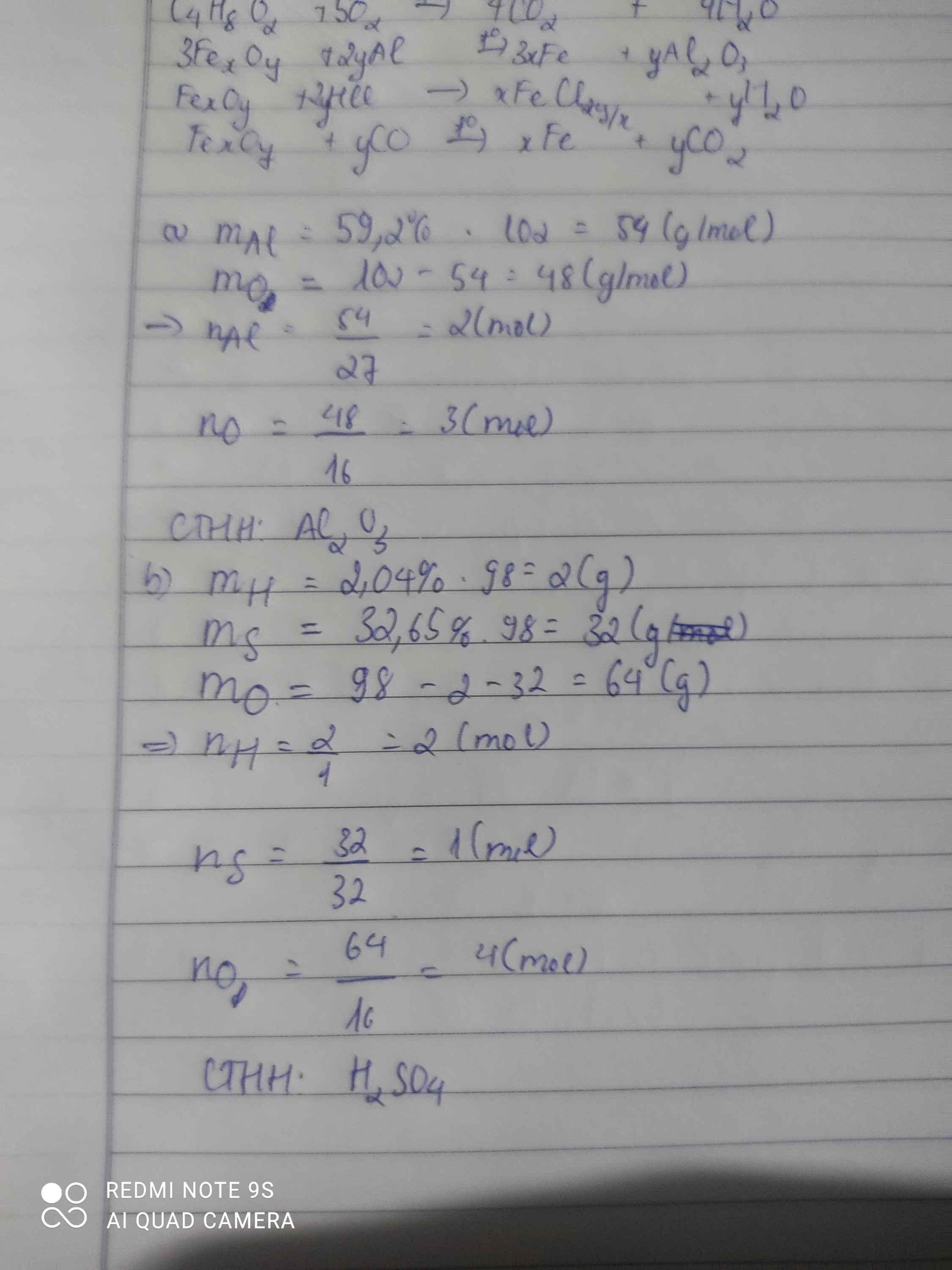
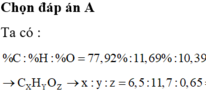
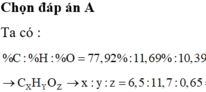
Chất này là KAl(OH)4. Còn cách giải thì mình chưa biết 😂😂😂