Một lượng vôi bị biến chất gồm CaCO3 và Ca(OH)2. Nung nóng A ở nhiệt độ cao thì khối lượng chất rắn còn lại bằng 60% khối lượng hỗn hợp ban đầu. Hãy tính % khối lượng hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
+ S ơ đ ồ p h ả n ứ n g : C a C O 3 M g O → t 0 ⏟ 30 g a m C a O M g O ⏟ 20 g a m + C O 2 ↑ ⇒ n C a C O 3 = n C O 2 = 30 - 20 44 ⇒ % m C a C O 3 = 10 . 100 44 . 30 = 75 , 76 %

Chọn A
Đề bài chỉ hỏi tỉ lệ giữa các khối lượng nên có thể lấy 90 gam hỗn hợp ban đầu và sau phản ứng còn lại
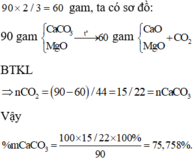

Đáp án A
Định hướng tư duy giải
Giả sử số mol CaCO3 trong hỗn hợp đầu là 1 mol
C a C O 3 → C a O + C O 2 ↑
m t r ư ớ c - m s a u = m C O 2 = m t r ư ớ c - 2 3 m t r ư ớ c
m t r ư ớ c = 3 m C O 2 = 132 g
% m C a C O 3 / h h = 75 , 76 %

Giả sử trong hỗn hợp ban đầu có 1 mol CaCO3 ⇒ nCO2 = 1
∆m = mtrước – msau ⇒ mCO2 = mtrước – 2/3mtrước = 1/3mtrước
⇒ mtrước = 3mCO2 = 3.44 = 132g
⇒ %mCaCO3 = 100 132 . 100 % = 75 , 76 % ⇒ Chọn A.

Tóm tắt: 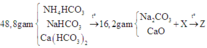
Gọi a; b; c lần lượt là số mol của NH4HCO3, NaHCO3 và Ca(HCO3)2
Ta có: 89a + 84b + 162c =48,8 (l)
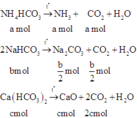
Khối lượng của hỗn hợp rắn là: 53b + 56c = 16,2 (2)
Hỗn hợp khí X gồm NH3 (a mol) và CO2 (a + b 2 + 2c)
⇒ n x = (2a + b 2 + 2c)
Khi X ở nhiệt độ 180 – 200°C, dưới áp suất khoảng 200 atm thì đây chính là phản ứng điều chế đạm urê nên ta có phản ứng:
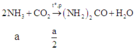
NH3 phản ứng với CO2 theo tỉ lệ 1:2 lượng khí Z còn lại chính là CO2 ⇒ n z = a 2 + b 2 . 2 c
Do sau phản ứng đưa về nhiệt độ ban đầu nên ta có:
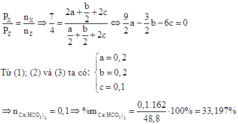
Đáp án A.

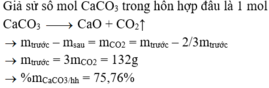
Coi mhh ban đầu = 100g
⇒%mAl2O3 = 1/8 * 100% = 12,5%
PTHH
CaCO3 ➜ CaO + CO2
MgCO3 ➜ MgO + CO2
Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y, ta có:
100x + 84y = (100 - 1/8 * 100) = 87,5 (1)
lại có:
(100 - mCO2) / 100 = [100 - 44(x+y)] / 100 = 6/10
⇒x + y = 0.91 (2)
Giải (1) và (2) ta được: x = 0,69125; y = 0,21875
%mCaCO3 = [(0,69125 * 100) / 100] * 100% = 69,125%
%mMgCO3 = 100% - 12,5% - 69,125% = 18,375%