Hòa tan hoàn toàn 5,95g hỗn hợp muối cacbonat của kim loại hóa trị I và kim loại hóa trị II trong dd HCl thì sinh ra 1,12l khí (đktc). Đem cô cạn dung dịch sau phản ứng thì thu được bao nhiêu (g) muối khan.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1.
RCO3 -> RO + CO2
Áp dụng ĐLBTKL ta có:
mRCO3=mRO+mCO2
=>mCO2=10-5,6=4,4((g)\(\Leftrightarrow\)0,1(mol)
VCO2=22,4.0,1=2,24(lít)
Theo PTHH ta có:
nRCO3=nCO2=0,1(mol)
MRCO3=\(\dfrac{10}{0,1}=100\)
=>MR=100-60=40
=>R là Ca
4.
R + H2SO4 -> RSO4 + H2
nH2=0,5(mol)
Theo PTHH ta có:
nR=nH2=0,5(mol)
MR=\(\dfrac{12}{0,5}=24\)
=>R là Mg

Đáp án D
Gọi công thức chung của hai muối cacbonat kim loại hóa trị II là RCO3
RCO3 → RO + CO2
Áp dụng định luật bảo toàn khối lượng ta có:
mCO2 = mRCO3 - mRO = 13,4 - 6,8 = 6,6 (g)
⇒ nCO2 = 0,15 mol
Ta có: nNaOH = 0,075 mol
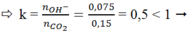
ð tạo ra muối NaHCO3 và CO2 dư.
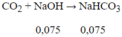
⇒mmuối = 0,075.84 = 6,3(g)

Gọi x, y lần lượt là số mol Zn và kim loại A. (x, y > 0)
PT theo khối lượng hỗn hợp:
65x + Ay = 1,7 (I)
Zn + 2HCl → ZnCl2 + H2
x//////2x///////////x///////////x
A + 2HCl → ACl2 + H2
y/////2y//////////y//////////y
nH2 = 0,03 (mol)
=> x + y = 0,03 (II)
nA = 1,9/A
nHCl = 0,1 (mol)
=> 1,9/A < 0,05
=> A > 38 (*)
Từ (I) và (II) có hệ phương trình, biến đổi hệ ta được:
y(65 – A) = 0,25
=> y = 0,25/(65 – A) => A < 65
Vì y < 0,03
=> 0,25/(65 – A) < 0,03
=> A < 56 (*) (*)
Từ (*) và (*) (*) ta có khoảng của A
38 < A < 56
=> A là Ca (40)

\(n_{Cu\left(NO_3\right)_2}=0,5.0,2=0,1\left(mol\right)\)
\(n_{NO_3^-}=0,1.2=0,2\left(mol\right)\)
\(n_{Cu^{2+}}=0,1\left(mol\right)\)
\(n_{HCl}=n_{H^+}=0,5.1,8=0,9\left(mol\right)\)
\(n_{NO}=\dfrac{n_{H^+}}{4}=\dfrac{0,9}{4}=0,225\left(mol\right)\)
Sau phản ứng thu được hỗn hợp kim loại \(\Rightarrow\) Cu và Fe \(\Rightarrow\) \(Fe^{2+}\)
Bảo toàn e:
\(2n_{Fe.pứ}=3n_{NO}+2n_{Cu^{2+}}\)
\(\Rightarrow n_{Fe.pứ}=0,4375\left(mol\right)\)
Có: \(a-m_{Fe.pứ}+m_{Cu}=m_{hh.kl}=0,5\)
\(\Leftrightarrow a-0,4375.56+64.0,1=0,5\\ \Rightarrow a=18,6\)

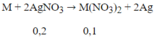

Ta có:
\(n_{CO_2}=\frac{1.12}{22.4}=0.05\left(mol\right)\) \(\Rightarrow m_{CO_2}=0.05\times44=2.2\left(g\right)\)
\(X_2CO_3+2HCl\rightarrow2XCl+H_2O+CO_2\)
\(YCO_3+2HCl\rightarrow YCl_2+H_2O+CO_2\)
Ta thấy
\(n_{HCl}=2n_{CO_2}=2\times0.05=0.1\left(mol\right)\)
\(\Rightarrow\) \(m_{HCl}=0.1\times36.5=3.65\left(g\right)\)
\(n_{H_2O}=n_{CO_2}=0.05\left(mol\right)\)
\(\Rightarrow\) \(m_{H_2O}=0.05\times18=0.9\left(g\right)\)
Áp dụng định luật bảo toàn khối lượng ta được:
\(m_{XCl+YCl_2}=\left(5.95+3.65\right)-\left(2.2+0.9\right)=9.6-3.1=6.5\left(g\right)\)