Cho m gam Na vào 50ml dung dịch AlCl3 1M.Sau khi phản ứng xảy ra hoàn toàn,thì thu được V lít khí đktc,dung dịch X và 1,56g kết tủa.Khi thổi Co2 dư vào dung dịch X lại thấy xuất hiện thêm kết tủa.Tính khối lượng Na ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Thổi CO2 vào vẫn thu được kết tủa nên trong X có Al(OH)4
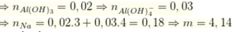

Chọn C.
Khi cho từ từ X vào KHSO4 thì:
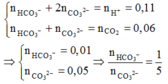
Khi Y tác dụng với Ba(OH)2 dư thì kết tủa thu được là
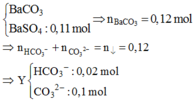
Vậy trong X có KHCO3 (0,03 mol) và Na2CO3 (0,15 mol) Þ m = 18,9 (g)

Chọn đáp án D
nH2SO4 = 0,156x0,5 = 0,078 Þ nH+ = 0,078x2 = 0,156
Cho từ từ 0,156 H+ vào

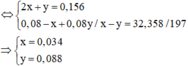
Vậy V = (0,034 + 0,088)x22,4=2,7328

8Al + 3Fe3O4 ---> 4Al2O3 + 9Fe
0,4<----0,15<------------0,2
Do sau phản ứng, cho dd vào NaOH thấy tạo H2--->Al dư <=> Fe3O4 hết.
X: Al2O3, Fe, Al dư
Al + NaOH + H2O ---> NaAlO2 + 3/2H2
0,1<--------------------------0,1<--. .... 0,15
Al2O3 + NaOH ----> NaAlO2 + H2O (2)
0,2<------------------------0,4
NaAlO2 + CO2 + H2O--->Al(OH)3 + NaHCO3
0,5<-----------------------------------0,5
nNaAlO2 (2) = 0,5-0,1=0,4
Tổng nAl=0,4 + 0,1=0,5
nFe3O4=0,15
--->m=48,3 g

Đáp án A
nOH- = 2nH2 = 0,06mol
=> nFe(OH)3 = 0,02mol
=> m = 2,14g

Đáp án A
nOH- = 2nH2 = 0,06mol
=> nFe(OH)3 = 0,02mol
=> m = 2,14g
nAlCl3=0.05.1=0.05mol
nAl(OH)3=1.56/78=0.02mol
PT:
2Na+2H2O-->2NaOH+H2
AlCl3+3NaOH-->Al(OH)3+3NaCl
0.05-->0.15------>0.05
Thổi khí CO2 vào dd X --> kết tảu => Trong X có ion AlO(-)
Gọi a là nAl(OH)3 tan trong NaOh dư
Al(OH)3+NaOh-->NaAlO2+2H2O
a----------->a
Ta có: nAl(OH)3 thu đc=0.05-a=0.02
< = > a=0.03mol
∑nNaOH=0.15+0.03=0.18mol
=>nNa=0.18mol
=>m=mNa=23.0.18=4.14g.
Na tác dụng với AlCl3 không tạo ra chất khí bạn à