cho lượng dư dung dịch AgNO3 vào một lít dung dịch hỗn hợp NaF 0,2M và NaCl 0,1M : a) tính khối lượng kết tủa thu được ; b) tính thể tích dung dịch AgNO3 1M đã dùng , biết rằng đã dùng dư 25%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\Sigma CM_{hh}=0,6M\)
\(\Rightarrow n_{hh}=0,18\left(mol\right)\)
Bao toàn Cl
\(5n_{Cl\left(hh\right)}=2n_{Cl\left(kt\right)}=\frac{0,18.5}{3}=0,3\left(mol\right)\)
\(\Rightarrow m_{AgCl}=43,05\left(g\right)\)

Chọn đáp án A
Kết tủa là AgCl.
n A g C l = n N a C l = 0,1.0,1 = 0,01 mol => m = 0,01.143,5 = 1,435 (gam)

Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
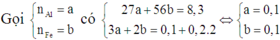
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO
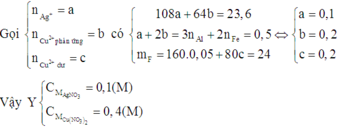

NaF không tạo kết tủa
\(AgNO_3+NaCl\rightarrow AgCl+NaNO_3\)
\(AgNO_3+NaBr\rightarrow AgBr+NaNO_3\)
\(n_{NaCl}=0,25.0,25=0,625\left(mol\right)=n_{AgCl}\)
\(n_{NaBr}=0,25.0,2=0,05\left(mol\right)=n_{AgBr}\)
\(\Rightarrow m\downarrow=m_{AgCl}+m_{AgBr}=0,0625.188+0,05.143,5=18,925\left(g\right)\)

Đáp án D
Kết tủa là AgCl
AgNO3 + NaCl → AgCl + NaNO3
=> nNaCl = nAgCl = 17,22/143,5 = 0,12 (mol)
=> %mNaF = ![]() .100 = 41,8%
.100 = 41,8%


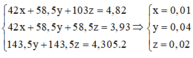
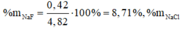
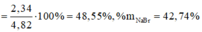
a) Chỉ có AgCl kết tủa, AgF không kết tủa nên khối lượng kết tủa thu được = 143,5.0,1 = 14,35 g.
b) Số mol AgNO3 = 0,3 mol, nên VAgNO3 p.ư = 0,3/1 = 300 ml.
Vì dùng dư 25% nên V = 300 + 300.0,25 = 375 ml.