Cho 100 ml dung dịch X gồm H2SO4 0,1M; HCl 0,2M; HNO3 0,3M tác dụng vừa đủ với V lít dung dịch Y chứa NaOH 0,2M và Bà(OH)2 0,1M. Tính V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
nH+ = 0,1(2. CMH2SO4 + CMHCl )= 0,02;
nNaOH = 0,1[CMNaOH + 2CMBa(OH)2] = 0,04.
H+ + OH- " H2O dư 0,02 mol OH-.
[OH-] = 0,02/(0,1+0,1) = 0,1 = 10-1.
[H+] = 10-13 ⇒ pH = 13

Đáp án A
Ta có nH+=0.02, nOH-=0.04 nên sau phản ứng nOH- = 0,02 và V = 0,2
→ Cm OH- = 0,1 => pH = 1

Chọn A
Ta có nH2SO4 = 0,05.0,1 = 0,005 mol; nHCl = 0,1.0,1 = 0,01 mol
⇒ ∑nH+ = 2nH2SO4 + nHCl = 2.0,005 + 0,01 = 0,02 mol
nNaOH = 0,2.0,1 = 0,02 mol; nBa(OH)2 = 0,1.0,1 = 0,01 mol
⇒ ∑nOH- = nNaOH + 2nBa(OH)2 = 0,02 + 2.0,01 = 0,04 mol
Khi trộn axit với kiềm thì bản chất của phản ứng là:
H+ + OH- → H2O
(0,02) (0,04)
⇒ nOH-còn dư = 0,04 – 0,02 = 0,02 mol ⇒ [OH-] còn dư = 0,02/0,2 = 0,1M
⇒ Dung dịch X có pOH = - lg[OH-]còn dư = 1 ⇒ pH = 14 – 1 = 13

Đáp án B
nOH- = 0,1.2.0,1 + 0,1.0,1 = 0,03
nH+ = 0,4.2.0,0375 + 0,4.0,0125 = 0,035
⇒ Trong X có H+ dư
⇒ nH+/X =0,035 – 0,03 = 0,005; VX = 100 + 400 = 500ml
⇒ [H+] = 0,01 ⇒ pH = 2.
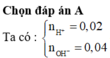
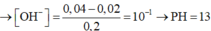


\(n_{H^+}=0,07mol=n_{OH^-}\)=>\(v=\dfrac{0,07}{0,2+0,1.2}=0,175l\)