Có một oxit sắt chưa rõ công thức, chia oxit này làm 2 phần bằng nhau.
a/ Để hoà tan hết phần 1 cần dùng150ml dung dịch HCl 1,5M.
b/ Cho luồng khí H2 dư đi qua phần 2 nung nóng, phản ứng xong thu được 4,2g sắt.
Tìm công thức của oxit sắt nói trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nO(Oxit)=\(\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,15.3=0,225mol\)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
-Gọi công thức là FexOy
-Ta có:
x:y=0,15:0,225=2:3\(\rightarrow\)Fe2O3

FexOy+2yHCl->xFeCl2y/x+yH2O
nHCl=0.225(mol)
->nFexOy=0.225*1/2y=0.225/2y
FexOy+yH2->xFe+yH2O
nFe=0.075(mol)->nFe=0.075*1/x=0.075/x
Vì lượng oxit sắt ở hai pt bằng nhau
->số mol oxit sắt cũng bằng nhau
->\(\frac{0.225}{2y}=\frac{0.075}{x}\)
->0.225x=2y*0.075
0.225x=0.15y
->x/y=0.15:0.225=2/3
->công thức của oxit sắt đó là Fe2O3

Ct FexOy
FexOy + 2yHCl ====xFeCl2y/x + yH2O
a.............2ay
=> 2ay = 0,45 => ay = 0,225
FexOy + yCO ====xFe + yCO2
a.............................ax
=> ax = 8,4/56 = 0,15
=> ay/ax = 0,225/0,15 = 3 : 2
=> Ct sắt oxit là Fe2O3

Đáp án A
Phần 1: Hỗn hợp tác dụng với HC1 gồm Al và FexOy
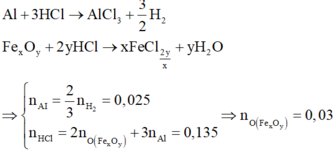
Phần 2: Có thể coi quá trình nhiệt nhôm với phản ứng xảy ra hoàn toàn như sau:

Vì phản ứng xảy ra hoàn toàn nên hỗn hợp sau phản ứng gồm Fe, A12O3 và Al dư. Khi cho hỗn hợp này vào dung dịch NaOH dư thì chất rắn còn lại là Fe.
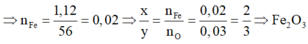

FexOy+2yHCl->xFeCl2y/x+yH2O
nHCl=0.225(mol)
->nFexOy=0.225*1/2y=0.225/2y
FexOy+yH2->xFe+yH2O
nFe=0.075(mol)->nFe=0.075*1/x=0.075/x
Vì lượng oxit sắt ở hai pt bằng nhau
->số mol oxit sắt cũng bằng nhau
->0.225/2y=0.07/5x
->0.225x=2y*0.075
0.225x=0.15y
->x/y=0.15:0.225=2/3
->công thức của oxit sắt đó là Fe2O3

gọi oxit sắt đó là FexOy
ta có pt :
1) FexOy + 2yHCl - > xFeCl2y/x + yH2O
theo đề : Vdd = 150ml ; CM = 1,5M
=> nHCl=0.225(mol)
theo pt:
->nFexOy=\(0,225.\dfrac{1}{2y}=\dfrac{0,225}{2y}\left(mol\right)\)
ta có pt:
2) FexOy + yH2 -> xFe + yH2O
theo đề ta có mFe = 4,2g
=> nFe = 0.075(mol) -> nFexOy=\(0,75.\dfrac{1}{x}=\dfrac{0,75}{x}\)
Vì lượng oxit sắt ở hai pt bằng nhau
-> nFexOy (1) = nFexOy (2)
->\(\dfrac{0,225}{2y}=\dfrac{0,75}{x}\)
->0.225.x=2y . 0.075
-> 0.225x=0.15y
->\(\dfrac{x}{y}=\dfrac{0,15}{0,225}=\dfrac{2}{3}\)
-> x = 2 ; y = 3
vậy công thức của oxit sắt đó là Fe2O3
chúc bạn học tốt
Gọi CTTQ: FexOy
Phần 1:
nHCl = 1,5 . 0,15 = 0,225 mol
Pt: FexOy + 2yHCl --> xFeCl2y/x + yH2O
\(\dfrac{0,225}{2y}\)<----0,225
Phân 2:
nFe = \(\dfrac{4,2}{56}=0,075\left(mol\right)\)
Pt: FexOy + yH2 --to--> xFe + yH2O
......\(\dfrac{0,075}{x}\)<--------------0,075
Ta có: \(\dfrac{0,225}{2y}=\dfrac{0,075}{x}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0,075.2}{0,225}=\dfrac{2}{3}\)
Vậy CTHH: Fe2O3

Đặt CTDC của oxit sắt: FexOy
Chia làm hai phần bằng nhau:
+ Phần 1:
\(Fe_xO_y\left(\dfrac{0,225}{y}\right)+2yHCl\left(0,45\right)--->xFeCl_{\dfrac{2y}{x}}+yH_2O\)\(\left(1\right)\)
\(n_{HCl}=3.0,15=0,45\left(mol\right)\)
\(Theo\left(1\right)\)\(n_{Fe_xO_y}=\dfrac{0,225}{y}\left(mol\right)\)
+ Phần 2:
\(yCO+Fe_xO_y\left(\dfrac{0,15}{x}\right)-t^o->xFe\left(0,15\right)+yCO_2\)\(\left(2\right)\)
\(n_{Fe}=0,15\left(mol\right)\)
Theo (2) \(n_{Fe_xO_y}=\dfrac{0,15}{x}\left(mol\right)\)
Ta có lượng oxit Fe trên được chia làm hai phần bằng nhau
\(\Rightarrow\dfrac{0,225}{y}=\dfrac{0,15}{x}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0,15}{0,225}=\dfrac{2}{3}\)
\(\Rightarrow\)CT của oxit Sắt cần tìm là: \(Fe_2O_3\)
niceee