Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=\frac{108\cdot1000}{27}=4000\left(mol\right)\)
PTHH : \(2Al_2O_3\underrightarrow{dpnc\left(criolit\right)}4Al+3O_2\)
Theo PTHH : \(n_{Al_2O_3}=\frac{1}{2}n_{Al}=2000\left(mol\right)\)
=> \(m_{Al_2O_3}=2000.102=204000\left(g\right)=204\left(kg\right)\)
Mà hiệu suất phản ứng là 80% => \(m_{Al_2O_3\left(thực\right)}=\frac{204}{80}\cdot100=255\left(kg\right)\)
=> \(m_{quặng}=\frac{255}{50}\cdot100=510\left(kg\right)\)

a. \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PTHH : Al2O3 + 6HCl -> 2AlCl3 + 3H2O
0,1 0,6 0,2 ( mol )
\(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
b.
PTHH : 3O2 + 4Al -> 2Al2O3
0,15 0,1 ( mol)
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
a. \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PTHH : Al2O3 + 3HCl -> 2AlCl3 + 3H2O
0,1 0,3 0,2 ( mol )
\(m_{HCl}=0,3.36,5=10,95\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
b.
PTHH : 3O2 + 4Al -> 2Al2O3
0,15 0,1 ( mol)
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)

a, PT: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2\)
b, Ta có: \(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=6n_{Al_2O_3}=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)

\(m_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.24,79=3,7185\left(l\right)\)

\(n_{H_2}=\dfrac{14,874}{24,79}=0,6\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
a, \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,4\left(mol\right)\Rightarrow m_{Al}=0,4.27=10,8\left(g\right)\)
b, \(n_{HCl}=2n_{H_2}=1,2\left(mol\right)\Rightarrow m_{HCl}=1,2.36,5=43,8\left(g\right)\)
\(n_{H_2}=\dfrac{14,874}{24,79}=0,6\left(mol\right)\)
PTHH :
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,4 1,2 0, 4 0,6
\(m_{Al}=0,4.27=10,8\left(g\right)\)
\(m_{HCl}=1,2.36,5=43,8\left(g\right)\)

Phương trình hóa học của phản ứng:
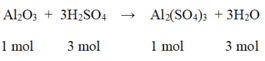
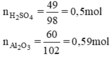
So sánh tỉ lệ 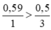 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
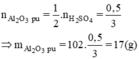
mAl2O3 (dư) = 60 - 17 = 43(g)

a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Gọi: mO2 = x (g) ⇒ mAl = 1,5x (g)
Theo ĐLBT KL, có: mAl + mO2 = mAl2O3
⇒ 1,5x + x = 10
⇒ x = 4 (g) = mO2
mAl = 1,5.4 = 6 (g)

\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,1--->0,3
=> mHCl = 0,3.36,5 = 10,95(g)
-
4Al+3NH4ClO4→2Al2O3+AlCl3+3NO+6H2O4Al + 3NH₄ClO₄ → 2Al₂O₃ + AlCl₃ + 3NO + 6H₂OPhương trình phản ứng:
-
-
-
-
soˆˊ mol Al=khoˆˊi lượng Alkhoˆˊi lượng mol của Al=1000g27g/mol≈37.04mol\text{số mol Al} = \frac{\text{khối lượng Al}}{\text{khối lượng mol của Al}} = \frac{1000 g}{27 g/mol} ≈ 37.04 molKhối lượng mol của các chất:
Al: 27 g/mol
NH₄ClO₄: 117.5 g/mol
Tính số mol của Al:
-
soˆˊ mol NH₄ClO₄=34×soˆˊ mol Al=34×37.04mol≈27.78mol\text{số mol NH₄ClO₄} = \frac{3}{4} \times \text{số mol Al} = \frac{3}{4} \times 37.04 mol ≈ 27.78 molTính số mol của NH₄ClO₄ cần dùng: Theo phương trình phản ứng, 4 mol Al phản ứng với 3 mol NH₄ClO₄.
-
khoˆˊi lượng NH₄ClO₄=soˆˊ mol NH₄ClO₄×khoˆˊi lượng mol của NH₄ClO₄=27.78mol×117.5g/mol≈3264.65g≈3.26kg\text{khối lượng NH₄ClO₄} = \text{số mol NH₄ClO₄} \times \text{khối lượng mol của NH₄ClO₄} = 27.78 mol \times 117.5 g/mol ≈ 3264.65 g ≈ 3.26 kgKhối lượng NH₄ClO₄ cần dùng:
Vậy, để phản ứng hoàn toàn với 1 kg Al, cần sử dụng khoảng 3.26 kg NH₄ClO₄.