Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tố Mg ở chu kì 3 nhóm IIA.
Nguyên tố Be ở chu kì 2 nhóm IIA.

Bài 3 :
3,72g X + H2O ---> X2O + 1,344 l H2
.....................................................0,06
Các quá trình cho nhận e :
Xo - 1e -> X+1
.........x................
2H+1 - 2e -> H2o
...........0,12.....0,06
ne cho = ne nhận => x = 0,12 ( mol )
Ta có :
Mx = \(\dfrac{3,72}{0,12}=31\)
=> \(\left\{{}\begin{matrix}M1< 31\\M2>31\end{matrix}\right.\)
=> Đó là Na(23) và K(39)
Bài 1 :
X có hạt nhân mang đt 17+
=> Z+ = 17
Ta có X có 3 lớp e và 7 e lớp ngoài cùng
Cấu hình e : 1s22s22p63s23p5
X là Cl ( Clo )
Vị trí :
- Nằm ở ô thứ 17 trong bảng tuần hoàn
- Chu kì 3 , nhóm VIIA

a) Cấu hình electron của A (Z=8): 1s22s22p4
=> Vị trí: Nhóm IVA, chu kì 2, ô số 8
b) Tính chất hoá học đặc trưng của A là tính oxi hoá. (Do A là phi kim)
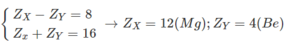
Tổng điện tích hạt nhân là : 31
\(p_X+p_Y=31\left(1\right)\)
Hai nguyên tố nằm ở hai nhóm kế tiếp nhau cùng chu kì nên :
\(p_X-p_Y=1\left(2\right)\)
\(\left(1\right),\left(2\right):p_X=16,p_Y=15\)
Y: Ô 16 , Chu kì 3 , Nhóm VIA
X : Ô 15 , Chu kì 3 , Nhóm VA
Số điện tích hạt nhân trung bình là 31 : 2 = 15,5
Vậy X và Y là P(15) và S(16)
X nằm ở ô 15 nhóm VA, chu kì 3
Y nằm ở ô 16 nhóm VIA, chu kì 3