Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt $n_{NO}=2a(mol);n_{NO_2}=a(mol)$
Bảo toàn e ta có: $6a+a=0,1.3+0,25.3\Rightarrow a=0,15(mol)$
Do đó $n_{A}=0,15.3=0,45(mol)\Rightarrow V_A=10,08(l)$
tham khảo trong:
https://moon.vn/hoi-dap/hoa-tan-hoan-toan-hon-hop-gom-01-mol-fe-va-025-mol-al-vao-dung-dich-hno3-du-thu-duoc-530914

Đáp án C.
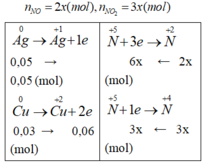
9x = 0,11; x= 11/900 => V = 5x.22,4 = 1,368 (l)

Theo gt ta có: $n_{NO}=n_{NO_2}=0,0175(mol)$
Quy hỗn hợp A về Fe và O với số mol lần lượt là a;b(mol)
Ta có: $56a+16b=5,04(g);3a-2b=0,07(mol)$
Suy ra $a=b=0,07$
Vậy x=0,07
Coi A gồm Fe(x mol) ; O(y mol)
Suy ra: 56x + 16y = 5,04(1)
Gọi : \(\left\{{}\begin{matrix}n_{NO}=a\left(mol\right)\\n_{NO_2}=b\left(mol\right)\end{matrix}\right.\)
Suy ra: \(\left\{{}\begin{matrix}a+b=0,035\\30a+46b=0,035.2.19\end{matrix}\right.\)
Suy ra: a = 0,0175 ; b = 0,0175
\(Fe^0 \to Fe^{+3} + 3e\\ 2e+O^0 \to O^{-2} \\ 3e + N^{+5} \to N^+{+2}\\ 1e + N^{+5} \to N^{+4}\)
Bảo toàn e :
3x = 2y + 0,0175.3 + 0,0175.1(2)
(1)(2) suy ra: x = 0,07 ; y = 0,07
Vậy x = 0,07

a)\(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64x+27y=9,1\\BTe:2x+3y=0,5\cdot1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,1\cdot64}{9,1}\cdot100\%=70,33\%\)
\(\%m_{Al}=100-70,33\%=29,67\%\)
b)\(\left\{{}\begin{matrix}n_{NO_2}+n_{NO}=0,5\\\dfrac{n_{NO_2}}{n_{NO}}=\dfrac{2}{1}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{NO_2}=\dfrac{1}{3}\\n_{NO}=\dfrac{1}{6}\end{matrix}\right.\)
Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64a+27b=9,1\\BTe:2x+3y=\dfrac{1}{3}\cdot1+\dfrac{1}{6}\cdot3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=\dfrac{4}{115}\\b=\dfrac{527}{2070}\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{\dfrac{4}{115}\cdot64}{9,1}\cdot100\%=24,46\%\)
\(\%m_{Al}=100\%-24,46\%=75,54\%\)
\(n_{HNO_3}=2n_{NO_2}+4n_{NO}=2\cdot\dfrac{1}{3}+4\cdot\dfrac{1}{6}=\dfrac{4}{3}mol\)

Coi \(n_{Cu} = n_{FeO} = 1(mol)\\ n_{Fe} = x(mol)\)
Bảo toàn electron cho quá trình 1:
\(2n_{Fe} + 2n_{Cu} = 3n_{NO}\)
⇒ 2x + 2 = 3a(1)
Y gồm \(Cu(NO_3)_2,Fe(NO_3)_2\)
Bảo toàn electron cho quá trình 2 :
\(n_{Fe(NO_3)_2} = x + 1 = 3n_{NO}\)
⇒ x + 1 = 3b(2)
Lấy (1) : (2), ta có \(\dfrac{2x + 2}{x + 1} =\dfrac{3a}{3b} \Rightarrow \dfrac{a}{b} = 2\)

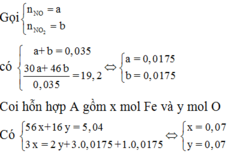




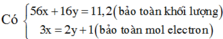
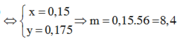
Ta dễ dàng tính được nFe = 0,05 mol, nFeO = 0,1 mol, nFe3O4 = 0,15 mol, nFe2O3 = 0,2 mol.
Khi cho lượng HNO3 tối thiểu thì Fe chưa td với HNO3. Có FeO, Fe3O4 và Fe2O3 tdung, Fe2O3 td không cho ra sp khử nên số mol Fe và O tham gia pứ OXH khử là trong FeO và Fe3O4.
\(Fe\left(0,55\right)\rightarrow Fe^{+3}+3e\left(1,65\right)\)
\(O\left(0,7\right)+2e\left(1,4\right)\rightarrow O^{-2}\)
\(N^{+5}+3e\left(3a\right)\rightarrow N^{+2}\left(a\right)\)
\(N^{+5}+1e\left(b\right)\rightarrow N^{+4}\left(b\right)\)
Bảo toàn e \(\Rightarrow1,4+3a+b=1,65\left(1\right)\)
\(n_Y=0,2\left(mol\right)\Rightarrow a+b=0,2\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=0,025\\b=0,175\end{matrix}\right.\)
=> Tỉ khối của Y so với O2 là 1,375 (g/mol)
\(n_{Fe\left(NO_3\right)_3}=2n_{Fe_2O_3}+n_{Fe^{3+}}=0,95\left(mol\right)\)
\(Fe\left(0,05\right)+2Fe\left(NO_3\right)_3\left(0,1\right)\rightarrow3Fe\left(NO_3\right)_2\left(0,15\right)\)
\(n_{HNO_3}=n_{NO_3^-\left(muoi\right)}+n_{N\left(khí\right)}=0,15.2+0,85.3+0,025+0,175=3,05\left(mol\right)\)
\(\Rightarrow V=0,7625\left(l\right)\)