Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Na2CO3 + 2HCl →2NaCl + CO2+ H2O
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Na2CO3 + Ba(NO3)2 → 2NaNO3 + BaCO3
Na2CO3 + Mg(OH)2 → 2NaOH + MgCO3
CaCO3 +2HCl → CaCl2 + CO2 +H2O
K2SO4 + Ba(OH)2 → 2KOH + BaSO4
K2SO4 + Ba(NO3)2 → 2KNO3 + BaSO4
2HCl + Ba(OH)2 → BaCl2 + 2H2O
2HCl + Ba(NO3)2 →BaCl2 + 2HNO3
2HCl + Mg(OH)2 → MgCl2 + 2H2O

câu 1:
các chất có thể tác dụng với nhau từng đôi một
KOH với HCl: KOH + HCl ➝ KCl + H2O
KOH với H2SO4 loãng: 2KOH + H2SO4 ➝ K2SO4 + 2H2O
KOH với AL2O3: 2KOH + Al2O3 ➝ 2KAlO2 + H2O
KOH với khí CO2: 2KOH + CO2 ➝ K2CO3 + H2O
hoặc KOH + CO2 ➝ KHCO3
HCl với Fe(OH)3: 6HCl + 2Fe(OH)3 ➝ 2FeCl3 + 6H2O
HCl với Al2O3: 6HCl + Al2O3 ➝ 2AlCl3 + 3H2O
H2SO4 với Fe(OH)3: 3H2SO4 + 2Fe(OH)3 ➝ Fe2(SO4)3 + 6H2O
câu 2:
HCl và H2SO4 loãng tác dụng được với kim loại tạo muối và khí H2:
HCl + Zn ➝ ZnCl2 + H2↑
H2SO4 + Zn ➝ ZnSO4 + H2↑
HCl và H2SO4 loãng tác dụng với oxit kim loại tạo muối và nước:
HCl + MgO ➝ MgCl2 + H2O
MgO + H2SO4 ➝ MgSO4 + H2O
còn lại là tương tự bạn tự giải nha ^^

a) Hiện tượng lần lượt là
- Sắt tan dần, xuất hiện khí không màu không mùi
$Fe +2 HCl \to FeCl_2 + H_2$
- Không hiện tượng gì
- $Fe_2O_3$ tan dần, dung dịch có màu nâu đỏ
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
- $MgO$ tan dần
$MgO + 2HCl \to MgCl_2 + H_2O$
- $Na_2SO_3$ tan dần, xuất hiện khí không màu mùi hắc
$Na_2SO_3 + 2HCl \to 2NaCl + SO_2 + H_2O$
- $CaCO_3$ tan dần, xuất hiện khí không màu không mùi
$CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O$
b)
Đốt quặng pirit thu được khí không màu mùi hắc
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
Cho vào dd brom : dung dịch brom nhạt màu rồi mất màu
$SO_2 + Br_2 + 2H_2O \to 2HBr + H_2SO_4$
Cho vào dd $H_2S$ : Xuất hiện kết tủa vàng
$2H_2S + SO_2 \to 3S + 2H_2O$

a,PTHH:
\(2CH_3COOH+CaCO_3\rightarrow\left(CH_3COO\right)_2Ca+CO_2\uparrow+H_2O.\)
b, Ta có :\(n_{CH_3COOH}=\dfrac{12}{60}=0,2mol\)
\(2CH_3COOH+CaCO_3\rightarrow\left(CH_3COO\right)_2Ca+CO_2\uparrow+H_2O.\)
0,2.........................................0,1
\(\Rightarrow m_{CaCO_3}\left(pu\right)=0,1.100=10g\)
c,
\(2CH_3COOH+CaCO_3\rightarrow\left(CH_3COO\right)_2Ca+CO_2\uparrow+H_2O.\)
0,2..........................................................................................0,1
\(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3\downarrow+H_2O\)
0,1.................................................0,1
Khối lượng kết tủa thu được : \(m_{BaCO_3}=0,1.197=19,7g\Rightarrow a=19,7\)


4FeS2 + 11O2 ------to----> 2Fe2O3 + 8SO2
\(H_2O-^{đp}\rightarrow H_2+\dfrac{1}{2}O_2\)
\(2NaCl+2H_2O-^{đpddcmn}\rightarrow2NaOH+Cl_2+H_2\)
\(Cl_2+H_2-^{t^o}\rightarrow2HCl\)
Điều chế Fe(OH)2
\(Fe_2O_3+H_2-^{t^o}\rightarrow Fe+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
Điều chế Fe(OH)3
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+H_2O\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
Điều chế Na2SO3
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
Điều chế NaHSO3
\(NaOH+SO_2\rightarrow NaHSO_3\)

\(a,CO_2+Ba(OH)_2\to BaCO_3\downarrow+H_2O\\ b,n_{CO_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ \Rightarrow n_{Ba(OH)_2}=0,1(mol)\\ \Rightarrow C_{M_{Ba(OH)_2}}=\dfrac{0,1}{0,2}=0,5M\\ c,n_{BaCO_3}=0,1(mol)\\ \Rightarrow m_{BaCO_3}=0,1.197=19,7(g)\)
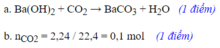
Có thể tạo thành muối acid, tuỳ vào lượng CO2.
a) không phản ứng
b)
* Nếu KOH dư tạo muối trung hoà
2KOH + CO2 → K2CO3 + H2O
* Nếu CO2 dư tạo muối axit
KOH + CO2 → KHCO3
c) không phản ứng
d)
* Nếu Ba(OH)2 dư tạo muối trung hoà
Ba(OH)2 + CO2 → BaCO3+ H2O
* Nếu CO2 dư tạo muối axit
Ba(OH)2 +2CO2 → Ba(HCO3)2