Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
pH = 11 => OH- dư sau phản ứng => pOH =3
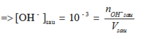
=> nOH- sau = Vsau . [OH-] = 10-3. 0,6= 0,0006 = 6.10-4 (mol)
pH = 2 => [H+]= 10-2 = 0,01M => nH+= 0,3 . 0,01= 0,003
nOH- = 0,3.a
H+ + OH- → H2O
Ban đầu: 0,003 0,3.a
Phản ứng: 0,003 0,003
Sau: 0 0,3.a-0,003
nOH- sau= 6.10-4 = 0,3a -0,003 => a=0,012M

a. nHCl = 10-2. 0,01 = 10-4 mol
=> Nồng độ H+ sau pha = 10-4: (0,09 + 0,01) = 10-3 => pH dd sau pha = 3
b. nồng độ H+ sau pha = [(10-2. 0,1) + (10-3. 0,1)] : 0,2 = 0,0055M
=> pH dd sau pha = -lg(0,0055) = 2,26
c. nOH- = 0,3. 0,01 = 0,003. nH+ = 0,2. 0,01 = 0,002
=> OH- dư = 0,003 - 0,002 = 0,001 => nồng độ OH- = 0,001: (0,3+0,2) = 0,002M => pOH = -lg0,002 = 2,7 => pH = 14 - 2,7 = 11,3

Đáp án B
nH+ ban đầu = 0,1.2.0,1 + 0,2.0,1 + 0,3.0,1 = 0,07
dung dịch C có pH=1 ⇒ nH+/C = 0,1.(0,3 + V)
⇒ nH+ ban đầu = nH+/C + nOH- ⇒ 0,07 = 0,1.(0,3 + V) + 0,2V +0,1.2V
⇒ V =0,08l

a) Ta có: \(\left\{{}\begin{matrix}n_{CuCl_2}=0,3\left(mol\right)\\n_{BaCl_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left[Cu\right]=\dfrac{0,3}{0,5}=0,6\left(M\right)\\ \Rightarrow\left[Ba\right]=\dfrac{0,1}{0,5}=0,2\left(M\right)\\ \Rightarrow\left[Cl\right]=\dfrac{0,3.2+0,1.2}{0,5}=1,6\left(M\right)\)

Chọn C