Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các phản ứng hoá học xảy ra trên hai đĩa cân :
CaCO 3 + 2 HNO 3 → Ca NO 3 2 + H 2 O + CO 2
MgCO 3 + 2 HNO 3 → Mg NO 3 2 + H 2 O + CO 2
Vị trí của hai đĩa cân trong thí nghiệm lần thứ nhất :
Số mol các chất tham gia ( 1 ) : n CaCO 3 = 20/100 = 0,2 mol bằng số mol HNO 3
Số mol các chất tham gia (2) : n MgCO 3 = 20/84 ≈ 0,24 mol nhiều hơn số mol HNO 3
Như vậy, toàn lượng HNO 3 đã tham gia các phản ứng (1) và (2). Mỗi phản ứng đều thoát ra một lượng khí CO 2 là 0,1 mol có khối lượng là 44 x 0,1 = 4,4 (gam). Sau khi các phản ứng kết thúc, 2 đĩa cân vẫn ở vị trí thăng bằng.

\(n_{Mg}=\dfrac{13.44}{24}=0.56\left(mol\right)\)
TN1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.56................................0.56\)
TN2 :
\(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O\)
\(x............................x\)
Vì cân thăng bằng nên :
\(m_{Mg}-m_{H_2}=m_{MCO_3}-m_{CO_2}\)
\(\Rightarrow13.44-0.56\cdot2=22-44x\)
\(\Rightarrow x=0.22\)
\(M_{MCO_3}=\dfrac{22}{0.22}=100\left(g\text{/}mol\right)\)
\(\Rightarrow M=100-60=40\left(g\text{/}mol\right)\)
\(M:Ca\)

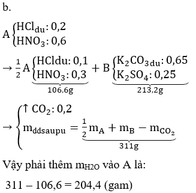
a.
|
|
AgNO3 |
K2CO3 |
| Ban đầu |
0,6 mol; 102 gam |
0,9 mol; 124,2 gam |
| Thêm vào |
→ HCl : 0 , 1 mol ↓ AgCl : 0 , 6 mol |
← H 2 SO 4 : 0 , 25 ↑ CO 2 : 0 , 25 |
| Sau phản ứng |
115,9gam |
213,2 gam |
| Thêm nước |
213,2 – 115,9 = 97,3 gam |
|

\(n_{Fe}=\frac{a}{56}\left(mol\right);n_{Al}=\frac{b}{27}\left(mol\right)\)
\(PT:Fe+2HCl\rightarrow FeCl_2+H_2\left(1\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\left(2\right)\)
\(n_{H_2\left(1\right)}=n_{Fe}=\frac{a}{56}\left(mol\right)\)
\(n_{H_2\left(2\right)}=\frac{3}{2}n_{Al}=\frac{b}{18}\left(mol\right)\)
Vì 2 cốc đựng dung dịch HCl và dung dịch H2SO4 ở vị trí thăng bằng, mà cho a gam Fe vào cốc đựng dung dịch HCl, cho b gam Al vào cốc đựng dung dịch H2SO4, cân vẫn ở vị trí thăng bằng nên \(m_{Fe}-m_{H_2\left(1\right)}=m_{Al}-m_{H_2\left(2\right)}\)
\(\Leftrightarrow a-\frac{a}{56}.2=b-\frac{b}{18}.2\)
\(\Leftrightarrow a-\frac{a}{28}=b-\frac{b}{9}\)
\(\Leftrightarrow\frac{27}{28}a=\frac{8}{9}b\)
\(\Rightarrow\frac{a}{b}=\frac{\frac{8}{9}}{\frac{27}{28}}=\frac{224}{243}\)

a) a(g) vào cốc CaCO3 xảy ra phản ứng:
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
b(g) vào cốc Cu xảy ra phản ứng:
\(Cu+H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
- Ở cốc 1 khối lượng tăng lên là (56/100)a. Ở cốc b khối lượng không thay đổi nên không thể xác định tỉ lệ a/b
b) \(CaCO_3+H_2SO_4\rightarrow CaSO_4+CO_2+2H_2O\)Cu vào cốc 1 không phản ứng.
Ở cốc 2, khối lượng tăng lên là: (56/100)a(g), cốc 2 tăng lên b(g)
Để cân thăng bằng thì (56/1000a=b=>a/b=100/56
ta có nCaCO3=25/100=0,25(mol)
gọi số g Al cần thêm vào là a(g) ---->mAl=a/27(mol)
PTHH:CaCO3+2HCl----->CaCl2+H2O+CO2 (1)
2Al+3H2SO4---->Al2(SO4)3+3H2 (2)
khối lượng của cốc A tăng là mCaCO3-mCO2=25-(0,25.44)=14(g)
khối lượng của cốc B tăng là mAl-mH2=a-(a/18.2)=a-a/9(g)
Muốn để cân thăng bằng thì 14=a-a/9 ---->a=15,75(g)
kl:vậy lượng nhôm cần thêm là 15,75g
cảm ơn!!-.-