Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Để giải bài toán này, chúng ta sẽ thực hiện các bước sau:
### Phần a: Tính số hạt mỗi loại của nguyên tử X
Gọi số proton, neutron và electron của nguyên tử X lần lượt là \( p, n, e \).
1. Tổng số hạt proton, neutron và electron là 52:
\[ p + n + e = 52 \]
2. Số hạt mang điện nhiều hơn số hạt không mang điện là 16:
\[ p + e - n = 16 \]
Vì nguyên tử trung hòa về điện tích, số proton bằng số electron:
\[ p = e \]
Do đó, chúng ta có thể thay \( e \) bằng \( p \) trong các phương trình trên:
\[ p + n + p = 52 \]
\[ 2p + n = 52 \quad \text{(1)} \]
\[ p + p - n = 16 \]
\[ 2p - n = 16 \quad \text{(2)} \]
Giải hệ phương trình (1) và (2):
Từ phương trình (1):
\[ n = 52 - 2p \]
Thay vào phương trình (2):
\[ 2p - (52 - 2p) = 16 \]
\[ 2p - 52 + 2p = 16 \]
\[ 4p - 52 = 16 \]
\[ 4p = 68 \]
\[ p = 17 \]
Vậy:
\[ p = 17 \]
\[ e = 17 \]
Thay vào phương trình (1) để tìm \( n \):
\[ 2p + n = 52 \]
\[ 2(17) + n = 52 \]
\[ 34 + n = 52 \]
\[ n = 18 \]
Vậy số hạt của nguyên tử X là:
- Proton: \( p = 17 \)
- Neutron: \( n = 18 \)
- Electron: \( e = 17 \)
### Phần b: Số electron trong mỗi lớp của nguyên tử X
Với số proton \( p = 17 \), nguyên tố X là Clo (Cl). Cấu hình electron của Cl là:
\[ 1s^2 2s^2 2p^6 3s^2 3p^5 \]
Do đó, số electron trong mỗi lớp là:
- Lớp 1: 2 electron
- Lớp 2: 8 electron
- Lớp 3: 7 electron
### Phần c: Tính nguyên tử khối của X
Nguyên tử khối của X là tổng khối lượng của các proton và neutron, vì khối lượng của electron rất nhỏ so với proton và neutron.
Khối lượng của X:
\[ \text{Nguyên tử khối} = p \cdot m_p + n \cdot m_n \]
\[ \text{Nguyên tử khối} = 17 \cdot 1.013 + 18 \cdot 1.013 \]
\[ \text{Nguyên tử khối} = 35 \cdot 1.013 \]
\[ \text{Nguyên tử khối} \approx 35.455 \]
### Phần d: Tính khối lượng bằng gam của X
Biết khối lượng của 1 đơn vị khối lượng nguyên tử (amu) là:
\[ 1 \, \text{amu} = \frac{1.9926 \times 10^{-23} \, \text{gam}}{12} \]
\[ 1 \, \text{amu} = 1.6605 \times 10^{-24} \, \text{gam} \]
Khối lượng của nguyên tử X bằng gam:
\[ \text{Khối lượng} \approx 35.455 \, \text{amu} \]
\[ \text{Khối lượng} \approx 35.455 \times 1.6605 \times 10^{-24} \, \text{gam} \]
\[ \text{Khối lượng} \approx 5.89 \times 10^{-23} \, \text{gam} \]
Vậy, khối lượng của nguyên tử X xấp xỉ \( 5.89 \times 10^{-23} \, \text{gam} \).

a) Theo đề bài ta có: \(p+n+e=34\) \(\Rightarrow2p+n=34\left(1\right)\)
Ta có: Số hạt mang điện nhiều hơn số hạt không mang điện là 10\(\Rightarrow p+e-n=10\Rightarrow2p-n=10\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}p=11\\n=12\end{matrix}\right.\)
\(\Rightarrow e=p=11\)
b) Nguyên tử khối của X: \(p+n=11+12=23\left(đvC\right)\)
Vậy X là Natri, kí hiệu là Na

Ta có: p + e + n = 52
Mà p = e, nên: 2p + n = 52 (1)
Theo đề, ta có: 2p - n = 16 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}2p+n=52\\2p-n=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=17\\n=18\end{matrix}\right.\)
Vậy p = e = 17 hạt, n = 18 hạt.
Vì tổng số hạt proton , nơtron , electron là 52 nên ta có :
\(p+n+e=52\Leftrightarrow2p+n=52\left(1\right)\)
Vì số hạt mang điện nhiều hơn số hạt không mang điện nên ta có :
\(2p-n=16\left(2\right)\)
Từ (1) và (2) ta có hệ phương trình :
\(\left\{{}\begin{matrix}2p+n=52\\2p-n=16\end{matrix}\right.\)
Giải hệ ta được :
\(p=17\Rightarrow e=17\)
\(n=18\)

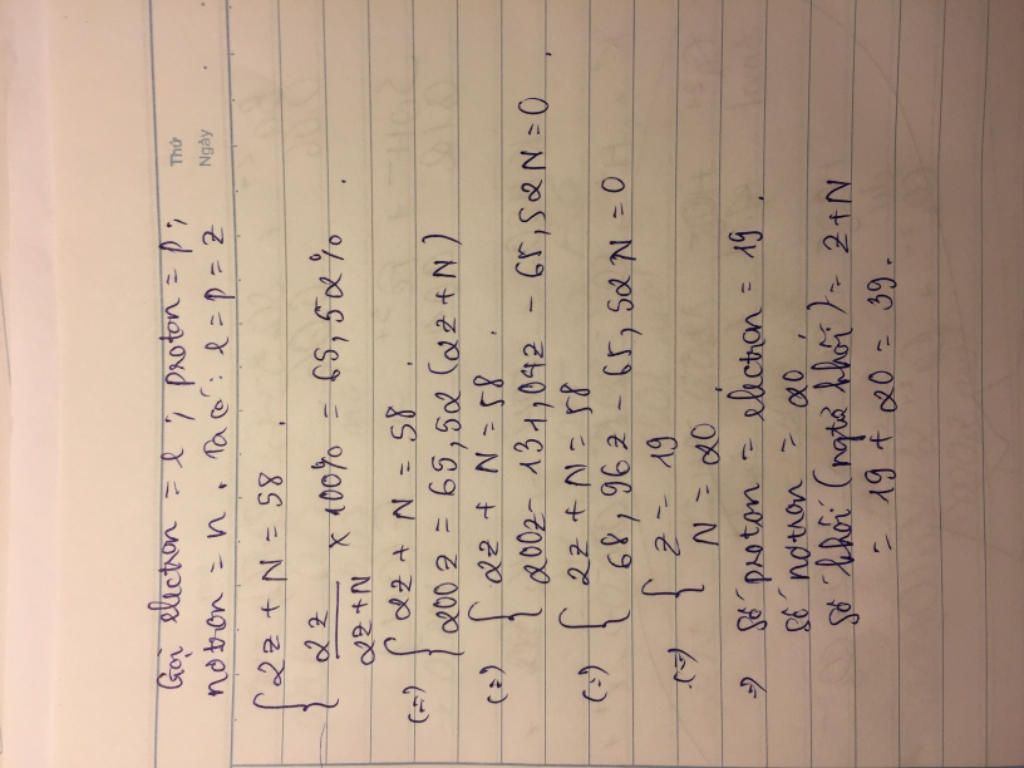
a) Theo đề bài ta có :
p + e + n = 60
Mà p = e = n => p = e = n = \(\dfrac{60}{3}=20\left(h\text{ạt}\right)\)
b) NTK của nguyên tử là :
NTK = p + n = 20 + 20 = 40 (đvc)
Vậy..............
Theo đề bài ta có :
n + p + e = 60 (hạt)
Vì n = p = e (đề bài )
=> 3n = 60
=> n = 20
=> n = p = e = 20 (hạt)
=> NTK của chất đó là : 40 (g/mol)
Vậy nguyên tử đó là Ca (Canxi)