Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình phản ứng khi đốt cháy cacbon:
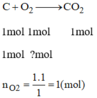
V O 2 = n O 2 .22,4 = 1.22,4 = 22,4(l)
→ V k k = 5 V O 2 = 5.22,4 = 112(l)

a)
\(n_P = \dfrac{62}{31} = 2(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ n_{O_2} = \dfrac{5}{4}n_P = 2,5(mol)\\ V_{O_2} = 2,5.22,4 = 56(lít)\\ V_{không\ khí} = \dfrac{56}{20\%} = 280(lít)\)
b)
\(n_P = \dfrac{31}{31} = 1(mol) ; n_{O_2} = \dfrac{23}{32} = 0,71875(mol)\\ \dfrac{n_P}{4} = 0,25 > \dfrac{n_{O_2}}{5} = 0,14375 \to P\ dư\\ n_{P\ pư} = \dfrac{4}{5}n_{O_2} = 0,575(mol)\\ m_{P\ dư} = 31 - 0,575.31 = 13,175(gam)\\ n_{P_2O_5} = \dfrac{2}{5}n_{O_2} = 0,2875(mol) \Rightarrow m_{P_2O_5} = 0,2875.142=40,825(gam)\)

Số mol Al tham gia pứ: 2,4.1022:6.1023=0,04mol
nO2=3/4.nAl=3/4.0,04=0,03mol
VO2=0,03.22,4=0,672l
-Thể ticsk kk tham gia : 0,672.5=3,36l
b)nAl2O3=2/4.nAl=2/4.0,04=0,02mol
mAl2O3=0,02.102=2,04g

nC = 1,8 : 12 = 0,15 (mol)
pthh : C+O2 --> CO2
0,15>0,15 (mol)
=> V O2 = 0,15 .22,4 = 3,36 (l)
=> Vkk = 3,36 : 1/5 = 16,8 (L)
nZn = 13 : 65 = 0,2 (mol)
pthh : 2Zn + O2 -t-> 2ZnO
0,2-----> 0,1 (mol)
=>VO2 = 0,1.22,4 = 2,24 (l)
=> Vkk = 2,24 : 1/5 = 11,2 (l)
nAl = 2,7 : 27 = 0,1 (mol)
pthh : 4Al + 3O2 --t--->2 Al2O3
0,1-->0,075 (mol)
=> VO2 = 0,075 . 22,4 = 1, 68 (l)
=> VKk = 1,68 : 1/5 = 8,4 (l)
a, nC = 1,8/12 = 0,15 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 0,15 ---> 0,3
Vkk = 0,3 . 5 . 22,4 = 33,6 (l)
b, nZn = 13/65 = 0,2 (mol)
PTHH: 2Zn + O2 -> (t°) 2ZnO
Mol: 0,2 ---> 0,1
Vkk = 0,1 . 5 . 22,4 = 11,2 (l)
c, nAl = 2,7/27 = 0,1 (mol)
PTHH: 2Al + 3O2 -> (t°) 2Al2O3
Mol: 0,1 ---> 0,075
Vkk = 0,075 . 5 . 22,4 = 8,4 (l)

-PTHH: \(4P+5O_2\rightarrow^{t^0}2P_2O_5\).
-\(n_P=\dfrac{m}{M}=\dfrac{3,1}{31}=0,1\left(mol\right)\)
-Theo PTHH trên, ta có:
-\(n_{O_2}=\dfrac{0,1}{4}.5=0,125\left(mol\right)\)
\(\Rightarrow V_{O_2}=n.22,4=0,125.22,4=2,8\left(l\right)\)
\(\Rightarrow V_{KK}=V_{O_2}.5=2,8.5=14\left(l\right)\)
\(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\\ 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\ n_{O_2}=\dfrac{5}{4}.0,1=0,125\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\\ V_{kk\left(đktc\right)}=2,8.5=14\left(l\right)\)

- nAl = N : 6.1023 = 2,4.1022:6.1023= 0,04
- Pt: 4Al + 3O2 -> 2Al2O3
-> nO2 = 0.03 mol ; nAl2O3 = 0,02 mol
a. VO2= n.22,4= 0,03.22,4 = 0,672 l
ta có Vkk = 5VO2 = 5.0,672 = 3,36l
b ta có m Al2O3= n.M=0,02 . 102 =2,04g

a)
\(4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Sản phẩm : Điphotpho pentaoxit.
b)
\(n_P = \dfrac{6,2}{31} = 0,2(mol)\\ \Rightarrow n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ \Rightarrow m_{P_2O_5} = 0,1.142 = 14,2(gam)\)
c)
\(n_{O_2} = \dfrac{5}{4}n_P = 0,125(mol)\\ \Rightarrow V_{O_2} = 0,125.22,4 = 2,8(lít)\)
d)
\(V_{không\ khí} = \dfrac{2,8}{20\%} = 14(lít)\)

a)
nP =62 : 31 = 2 (mol)
PTHH:4P + 5O2 --(to)-> 2P2O5
Theo PTHH: \(nO_2=\dfrac{5}{4}nP=\dfrac{5}{4}.2=2,5\left(mol\right)\)
VO2(đktc) = 2,5 ×22,4=56 (lít)
\(\dfrac{100\%}{21\%}.56=227\left(lít\right)\)
b)
\(nP=\dfrac{15,5}{31}=0,5\left(mol\right)\)
\(nO_2=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
0,4 0,5 0,2
tính theo pthh : => P dư , O2 đủ
nP(dư) = 0,5-0,4=0,1(mol)
=> mP (dư) = 0,1 . 31 = 3,1(g)
mP2O5 = 0,5 . 142=71(g)

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia p.ứng là :
nS = 3,2/32 = 0,1 (mol)
Theo phương trình ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VSO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% thể tích của không khí nên thể tích không khí cần là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
a)Phương trình phản ứng hóa học :
\(S+O_2->SO_2\)
b)Số mol lưu huỳnh thangia phản ứng
\(n_s\) =\(\frac{3,2}{32}\) =0,1(mol)
theo phương trình ta có
\(n_{so2}=n_s=n_{o2}\)
Thể tích khí sunfurơ sing ra được ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
tương tự thể tích khí cần dùng ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
Vì khí õi chiếm 20% về thể tích của không khí veentheer tích không khí cầ dùng là
\(V_{kk}=5.v_{o2}=5.2,24=11,2\left(l\right)\)
Chúc bạn học tốt ![]()
![]()
Phương trình hóa học khi đốt cháy photpho:
Thể tích của oxi cần: V O 2 = n O 2 .22,4 = 1,875.22,4 = 42(l)
Thể tích của không khí cần dùng là: V k k = 5 V O 2 = 5.42=210(l)