Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
\(m_N=\dfrac{14.17}{14+3}=14\left(g\right)\Rightarrow n_N=1\left(mol\right)\)
\(m_H=\dfrac{3.17}{14+3}=3\left(g\right)\Rightarrow n_H=3\left(mol\right)\)
2.
\(m_{Ag}=\dfrac{108.1,7}{108+14+16.3}=1,08\left(g\right)\Rightarrow n_{Ag}=0,01\left(mol\right)\)
\(m_N=\dfrac{14.1,7}{108+14+16.3}=0,14\left(g\right)\Rightarrow n_N=0,01\left(mol\right)\)
\(m_O=\dfrac{16.3.1,7}{108+14+16.3}=0,48\left(g\right)\Rightarrow n_O=0,03\left(mol\right)\)
3.
\(m_N=\dfrac{14.2.13,3}{\left(14+4\right).2+32+16.4}=2,82\left(g\right)\Rightarrow n_N=0,2\left(mol\right)\)
\(m_H=\dfrac{4.2.13,3}{\left(14+4\right).2+32+16.4}=0,81\left(g\right)\Rightarrow n_H=0,81\left(mol\right)\)
\(m_S=\dfrac{32.13,3}{\left(14+4\right).2+32+16.4}=3,22\left(g\right)\Rightarrow n_S=0,1\left(mol\right)\)
\(m_O=\dfrac{16.4.13,3}{\left(14+4\right).2+32+16.4}=6,45\left(g\right)\Rightarrow n_O=0,4\left(mol\right)\)

\(1,+n_{fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
số nguyên tử của Fe là 0,1.6.10\(^{23}\)=0,6.10\(^{23}\)
=> số nguyên tử của Zn là 3.0,6.10\(^{23}\)=1,8.10\(^{23}\)
+ n\(_{zn}\)= \(\dfrac{1,8.10^{23}}{6.10^{23}}\)=0,3 mol
=> m \(_{Zn}\)=0,3.65=19,5g ( đpcm)

a)
\(n_{Al}=0,2.2=0,4\left(mol\right)\)
\(n_S=0,2.3=0,6\left(mol\right)\)
\(n_O=0,2.12=2,4\left(mol\right)\)
b)
\(n_N=0,5.2=1\left(mol\right)\)
\(n_H=0,5.4=2\left(mol\right)\)
\(n_O=0,5.3=1,5\left(mol\right)\)

(1)gam/mol.
(2)6,022.1023.
(3)một.
(4)gam.
(5)trị số/ giá trị.
(6)đơn vị đo.
(7)phân tử khối.
(8)khác nhau.
Chúc bạn học tốt!
1, nguyên tử khối - một
2, gam/mol
3, giá trị - phân tử khối - khác nhau

Như vậy, khối lượng mol của một chất là khối lượng tính bằng gam của ..6,022.1023.nguyên tử hay phân tử hay của một mol chất.
Đơn vị đo khối lượng mol là gam/mol
Đối với mỗi nguyên tố, khối lượng mol nguyên tử và nguyên tử khối có cùng số trị/giá trị , khác nhau về đơn vị Đối với mỗi chất, khối lượng mol phân tử và phân tử khối có cùng trị số,giá trị về đơn vị đo.

Như vậy, khối lượng mol của một chất là khối lượng tính bằng gam của 6,022.1023 nguyên tử hay phân tử hay của một mol chất.
Đơn vị đo khối lượng mol là gam/mol.
Đối với mỗi nguyên tố, khối lượng mol nguyên tử và nguyên tử khối có cùng trị số/ giá trị, khác nhau về đơn vị đo. Đối với mỗi chất, khối lượng mol phân tử và phân tử khối có cùng trị số, khác nhau về đơn vị đo.

a)
\(m_C=\dfrac{52,15.46}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{13,04.46}{100}=6\left(g\right)=>n_H=\dfrac{6}{1}=6\left(mol\right)\)
\(m_O=46-24-6=16\left(g\right)=>n_O=\dfrac{16}{16}=1\left(mol\right)\)
=> CTHH: C2H6O
b) \(n_A=\dfrac{18,4}{46}=0,4\left(mol\right)\)
mC = 12.0,4.2 = 9,6(g)
mH = 1.0,4.6 = 2,4 (g)
mO = 16.0,4.1 = 6,4 (g)
c) \(n_A=\dfrac{13,8}{46}=0,3\left(mol\right)\)
Số nguyên tử C = 2.0,3.6.1023 = 3,6.1023
Số nguyên tử H = 6.0,3.6.1023 = 10,8.1023
Số nguyên tử O = 1.0,3.6.1023 = 1,8.1023

Số nguyên tử C trong 1,5 mol C6H12O6:
\(6.1,5.6.10^{23}=54.10^{23}\left(nguyên.tử\right)\)
Số nguyên tử H trong 1,5 mol C6H12O6:
\(12.1,5.6.10^{23}=108.10^{23}\left(nguyên.tử\right)\)
Số nguyên tử O trong 1,5 mol C6H12O6:
\(6.1,5.6.10^{23}=54.10^{23}\left(nguyên.tử\right)\)
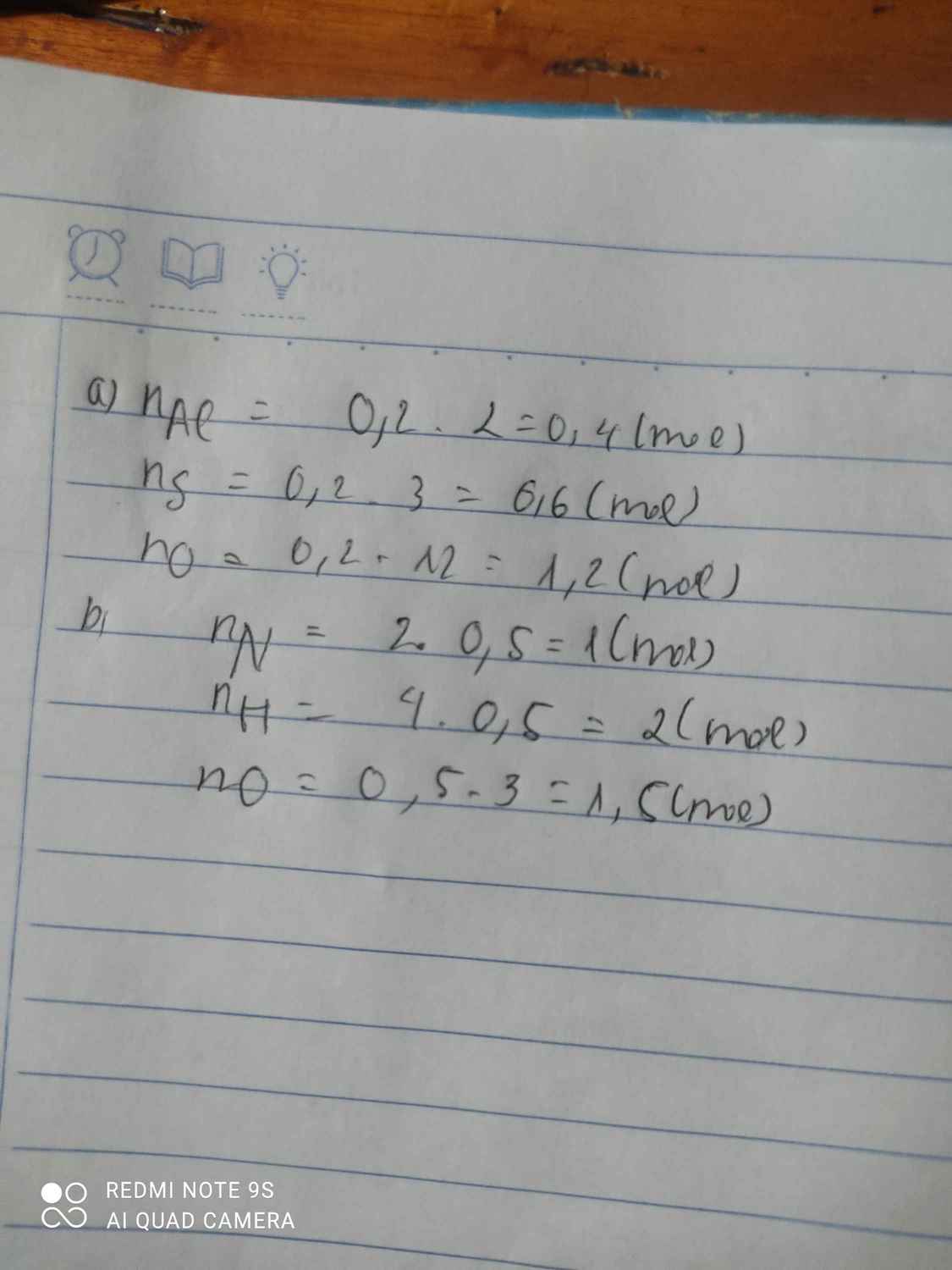
Số mol của NH3: nNH3 = 17 / 17 = 1 (mol)
=> Số mol N: nN= 1 (mol)
Số mol H: nH = 3 (mol)
theo đề có mNH3=17(g)
mà lại có MNH3=14+1*3=17(g/mol)
nên ADCT chuyển đổi giữa số mol và khối lg có
nNH3=\(\frac{m_{NH_3}}{M_{NH_3}}\) =17/17=1(mol)
theo CTHH có trong 1 mol h/c NH3 có 1 mol nguyên tử nguyên tố N và 3 mol nguyên tử nguyên tố H