Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tham khảo:
- Hiện tượng: Nước bromine mất màu và xuất hiện kết tủa trắng.
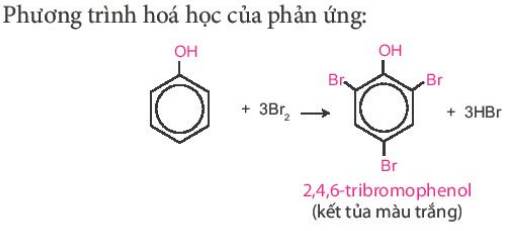
- Giải thích: Phenol phản ứng bromine, làm nước bromine mất màu, tạo kết tủa trắng 2,4,6-tribromophenol.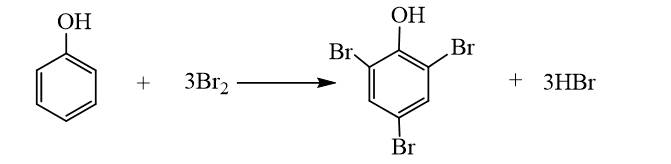
Hiện tượng:
-Nước brom mất màu
-Xuất hiện kết tủa trắng
Giải thích: Khi phenol phản ứng với brom thì sẽ làm mất màu nước brom và sẽ tạo ra kết tủa trắng 2,4,6-tribromophenol

Tham khảo:
- Phenol ít tan trong nước lạnh.
- Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt.
- Giải thích: Phenol phản ứng với dung dịch sodium hydroxide tạo thành dung dịch muối tan trong suốt sodium phenolate (C6H5ONa).
C6H5OH + NaOH → C6H5ONa + H2O
Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt
Giải thích: Phenol khi tác dụng với NaOH sẽ cho ra dung dịch muối tan trong suốt là C6H5ONa

Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt

Hiện tượng: Cả 2 ống nghiệm đều xuất hiện kết tủa xanh lam nhạt (Cu(OH)2)
PTHH: CuSO4 + 2 NaOH → Cu(OH)2↓(xanh) + Na2SO4 (PTHH ở bước 2)
- Khi cho gylycerol vào ống 1: Kết tủa tan tạo thành dung dịch màu xanh lam của muối copper(II) glycerate
PTHH: 2 C3H5(OH)3 + Cu(OH)2→ [C3H5(OH)2O]2Cu + 2 H2O
- Khi cho ethanol vào ống 2: không có hiện tượng, kết tủa không tan.
Hiện tượng
-Khi cho vào hai ống nghiệm dung dịch CuSO4 thì sẽ xuất hiện kết tủa màu xanh lam
-Khi cho vào ống 1 glyxerol thì sẽ làm cho kết tủa tan dần tạo dần thành dung dịch màu xanh lam
-Khi cho etanol vào ống 2 thì kết tủa sẽ ko tan
PTHH:
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)

Tham khảo:
- Khi nhỏ vài giọt dung dịch acetic acid lên mẩu giấy quỳ tím, mẩu quỳ tím hóa đỏ vì acetic acid có tính acid.
- Khi cho vào ống nghiệm thứ nhất chứa dung dịch acetic acid vài mẩu magnesium, mẩu magnesium tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với magnesium, làm magnesium tan và tạo khí hydrogen.
2CH3COOH + Mg → 2(CH3COO)2Mg + H2↑
- Khi cho vào ống nghiệm thứ hai chứa acetic acid 1 thìa sodium carbonate, sodium carbonate tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với sodium carbonate, sinh ra khí carbon dioxide.
2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2↑

Bài 6:
KMnO4 và HCl trong thí nghiệm được dùng để điều chế chlorine
2 KMnO4 + 16 HCl → 2 KCl + 2 MnCl2 + 5 Cl2 + 8 H2O
Bài 5:
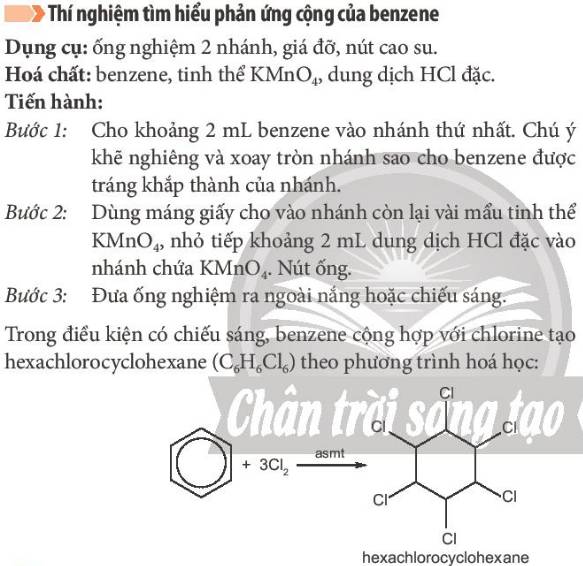
Hiện tượng: xuất hiện khói trắng, trên thành thấy xuất hiện một lớp bột màu trắng (Hexachlorocyclohexane).
C6H6 + 3 Cl2 -> (as) C6H6Cl6

Cồn cháy được tạo thành khí không màu và hơi nước.
Hiện tượng là etanol cháy tạo thành ngọn lửa màu vàng và nó sẽ tỏa nhiệt rất nhiều

Tham khảo:
Giải thích: Muối sodium phenolate phản ứng với hydrochloric acid tạo thành phenol và sodium chlordie. Phenol không tan do đó chất lỏng trong ống nghiệm phân thành 2 lớp.
Phương trình: C6H5ONa + HCl → C6H5OH + NaCl.
Muối C6H5ONa khi tác dụng thêm với Axit HCl sẽ tạo thành phenol và NaOH. Và vì phenol ko tan được nên chất lỏng trong ống nghiệm sẽ chia thành 2 lớp
\(C_6H_5ONa+HCl\rightarrow C_6H_5OH+NaCl\)










Tham khảo:
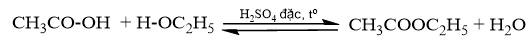
- Hiện tượng: Dung dịch sau phản ứng phân thành 2 lớp, có mùi thơm nhẹ.
- Phương trình:
- Dấu hiệu nhận biết có sản phẩm mới được tạo thành: Dung dịch bị phân lớp, xuất hiện mùi. Vì ester sinh ra ít tan trong nước, nhẹ hơn nước, nổi lên trên và có mùi thơm đặc trưng.