Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A.
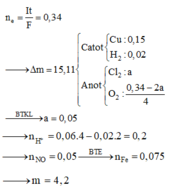
Phương trình điện phân:
Catot: Cu2+ + 2e → Cu
2H2O + 2e → H2 + 2OH-
Anot: 2Cl- → Cl2 + 2e
2H2O → 4H+ + O2 + 4e
Fe + dung dịch sau điện phân → NO
=> Chứng tỏ dung dịch chứa H+, ở anot đã xảy ra điện phân nước.
![]()
=> Chứng tỏ Cu2+ chưa bị điện phân hết


Chọn đáp án A
Xét t(s): Khối lượng catot tăng ⇒ ion M2+ bị điện phân. Khí duy nhất ở anot là Cl2.
2Cl– → Cl2 + 2e ⇒ ne = nNaCl = 2nCl2 = 0,4 mol ⇒ mMSO4 = 43,24 - 0,4 × 58,5 = 19,84(g).
Xét 2t(s): ne = 0,8 mol || 2H2O → 4H+ + O2 + 4e ⇒ nO2 = 0,1 mol.
⇒ manot giảm = 0,2 × 71 + 0,1 × 32 = 17,4(g) ⇒ mcatot giảm = 8,096(g).
Đặt nMSO4 = x ⇒ (M + 96).x = 19,84 (1) || 2H2O + 2e → 2OH– + H2
⇒ nH2 = (0,8 – 2x) ÷ 2 = 0,4 – x ⇒ 2 × (0,4 – x) + M.x = 8,096 (2)
(1) và (2) ⇒ M.x = 7,552 và x = 0,128 ⇒ M = 7,552 ÷ 0,128 = 59 (Ni).

Đáp án B
Giả sử tại anot chỉ có
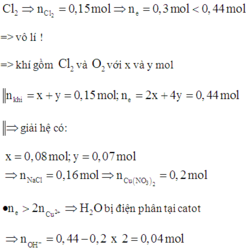
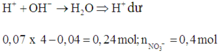
Xét Fe+ dung dịch sau điện phân: do thu được rắn =>Fe dư => Fe chỉ lên số oxi hóa +2
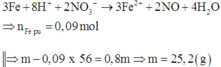

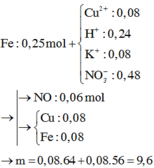




Chọn đáp án A