Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Quá trình CO phản ứng với oxit chỉ là CO lấy đi O tạo CO2 nên số mol O bị lấy cũng chính bằng số mol CO2. Vì Ca(OH)2 dư ⟹ nCO2 = 34,8/100 = 0,348 = nO bị lấy
⟹ nFe trong oxit = (18,56 – 0,348×16)/56=0,232
⟹ n F e n O = 0 , 232 0 , 348 = 2 3 ⟹ Fe2O3
yCO+FexOy--t°--> yCO2+xFe
CO2+Ca(OH)2--->CaCO3+H2O nCaCO3=34,8/100=0,348(mol
Theopt2: nCO2=nCaCO3=0,348(mol)
Theo pt1:
nFexOy=1/y.nCO2=0,348/y (mol)
MFexOy=18,56/0,348/y=160y/3(g/mol)
=>56x+16y=160y/3
168x+48y=160y
168x=112y
=>x/y=112/168=2/3
Vậy công thức hoá học của Oxt sắt là Fe2O3

Đáp án B
Định hướng tư duy giải:
Chất rắn X gồm: Al2O3, Cu, MgO, Fe vì vậy khi hòa tan vào dung dịch HCl loãng dư chỉ thu được 3 muối là MgCl2, AlCl3, FeCl2 (phản ứng không tạo Fe3+ nên không thể hòa tan Cu).

Đặt số mol Fe2O3 = a, Số mol CuO = b, ta có 160a + 80b = 25,6
2a . 242 + b . 188 = 73,12
=> a = 0,12; b = 0,08 => nO = 0,44
=> nCO2 = 0,44
=> m = 86,68 gam
=> Đáp án B

n CO2= 0,4 => n 0/oxit = 0,4
n fe= n H2= 0,2
=> m fe203 = 0,1 => n CuO= 0,1
=> m =

A
Ta có nO = nCaCO3 = 1,5.10-3.
Vậy m = 2,15 + 16. 1,5.10-3 = 2,174 gam

Đáp án D
Khi A tác dụng với CO thì: nO (pư) = nCO (pư) =0,125 mol
nNO = 0,09 mol, nHNO3 = 0,69 mol
Xét 2 trường hợp:
TH1: dung dịch C chứa Fe(NO3)3 + HNO3 (có thể dư)
Qui đổi hỗn hợp B thành Fe và O: F e : x m o l O : y m o l
Bảo toàn e ta có: 3x – 2y = 3nNO và 56x + 16y = 16,568 – 0,125.16 = 14,568
Giải hệ ⇒x = 0,2091 và y = 0,17865 mol ⇒ Số mol N sử dụng Fe(NO3)3: 0,2091 và NO: 0,09
Theo BTN: nN = 0,02091.3 + 0,09 = 0,7173 > 0,69 mol ⇒ loại
TH2: HNO3 hết, dung dịch C chứa 2 muối Fe(NO3)3 hoặc Fe(NO3)2
- Bảo toàn H: nH2O = 0,0345 mol
- Bảo toàn oxi cho toàn quá trình
y = (0,69 – 0,09).3 + 0,09.1 + 0,345 - 0,69.3 = 0,165 ⇔ 56x + 16y = 14,568 ⇔ x = 0,213 mol
Ta có:
→ a + b = 0,213
→ 3a+2b = 0,69 – 0,09 = 0,6
a =0,174; b=0,039
m = 0,174.107 + 0,039.90 = 22,128 gam

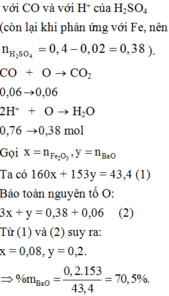

Chọn đáp án C