Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Cho nước vào 4 ống nghiệm đựng 4 chất :
+ Tan Na2CO3 , KCl => Sục HCl vào , sủi bọt khí Na2CO3 , không hiện tượng KCl
+Rắn BaSO4 , MgCO3 => Sục HCl vào , sủi bọt khí MgCO3 , không hiện tượng BaSO4
b) Cho nước vào 3 ống nghiệm đựng 3 chất
+Tan : K2CO3
+Rắn : BaCO3 , CaSO4 Sục HCl vào => sủi bọt khí BaCO3 , không hiện tượng CaSO4
c) d) tương tự
Lưu ý gốc \(CO^{2-}_3\) gặp axit sẽ tạo khí CO2
\(BaSO_4,CaSO_4,MgCO_3,CaCO_3\) Là rắn không tan , còn mấy cái kia là dugn dịch , cho nước để tách 2 nhóm rồi dùng HCl

Thành phần chính của quặng đôlomit là: C a C O 3 . M g C O 3 .
Đáp án cần chọn là: B

Đáp án là C.
Ca(HCO3)2![]() CaO + 2CO2 + H2O
CaO + 2CO2 + H2O
CaCO3![]() CaO + CO2
CaO + CO2
2NaHCO3![]() Na2CO3 + CO2 + H2O
Na2CO3 + CO2 + H2O

Đáp án B.
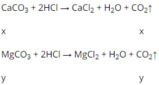
Số mol CO2: 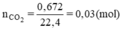
Gọi x, y lần lượt là số mol của CaCO3 và MgCO3 trong hỗn hợp
Theo bài ra ta có hệ phương trình:
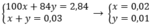
%mNa = 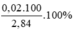 = 70,42%
= 70,42%
%mK = 100% - 70,42% = 29,58%

Na2CO3 không bị nhiệt phân, nên 2,24 lít khí sinh ra chính là CO2 do CaCO3 bị nhiệt phân theo phản ứng
![]()
Cách 1:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
m X = m c h ấ t r ắ n + m C O 2 = 11,6 + 0,1.44 = 16 (gam)
Vậy phần trăm khối lượng của CaCO3 trong hỗn hợp X là:
![]()
Cách 2:
Ta có:
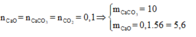
Hỗn hợp rắn thu được gồm CaO và Na2CO3
![]()
![]()
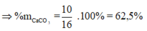
Đáp án D

Đáp án D
nCO2= nCaCO3 = 0,15 mol
ð mCaCO3 = 15 gam
mX= mrắn + mCO2
= 17,4+ 0,15.44=24 gam
%mCaCO3= (15:24).100%=62,5%



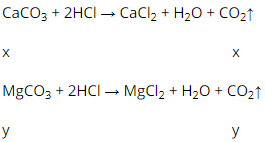
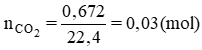
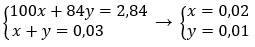
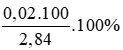 = 70,42%
= 70,42%
Giải thích: Đáp án B