Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

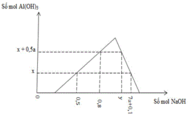
Chọn C
nNaOH = 1,1 mol
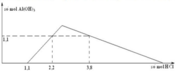
H2O + AlO2- + H+ → Al(OH)3
y y y
Al(OH)3 + 3H+ → Al3+ + 3H2O
y – 1,1 3y – 3,3
=> y + 3y - 3,3 = 2,7
=> 4y = 6 => y = 1,5

Đáp án A.
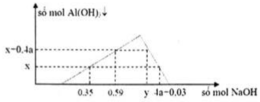
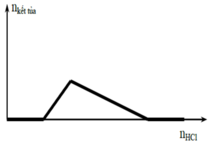
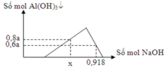
Nhỏ dung dịch HCl vào dung dịch A, lúc đầu chưa xuất hiện kết tủa ngay, sau đó xuất hiện kết tủa, kết tủa tăng dần đến cực đại rồi tan dần ra đến hết; đồ thị không cân đối nên A chứa NaOH và NaAlO2.

Chọn A
Khi cho dd OH- vào hỗn hợp gồm H+ và muối Al3+
Sẽ xảy ra các phản ứng hóa học theo thứ tự sau:
(1) OH- + H+ → H2O
(2) OH- + 3Al3+ → Al(OH)3↓
(3) OH- + Al(OH)3↓ → AlO2- + 2H2O
Khi phản ứng (1) kết thúc , bắt đầu xảy ra (2) thì xuất hiện kết tủa => đồ thị bắt đầu đi lên
Khi đồ thị đi lên từ từ đến điểm cực đại => xảy ra phản ứng (1) và (2)
Ta có công thức nhanh: nOH- = 3n↓ + nH+
Khi đồ thị bắt đầu đi xuống => phản ứng (3) xảy ra, kết tủa bắt đầu bị hòa tan dần dần đến hết
=> Ta có công thức tính nhanh: nOH- = 4nAl3+ - n↓ + nH+
Từ đây ta có các phương trình sau:
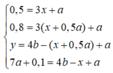
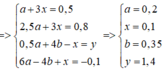
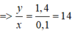

Đáp án : B
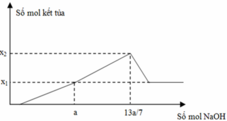
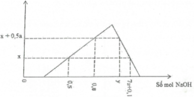
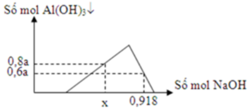
Tại nNaOH = 0,918 mol thì đồ thị đi xuống => kết tủa tan dần
=> nAl(OH)3 = 4nAl3+ - (nOH – nH+) => 0,6a = 4a – (0,918 – 2a)
=> a = 0,17 mol
Tại nNaOH = x mol đồ thị đi lên => Al3+ dư
=> 3nAl(OH)3 + nHCl = nNaOH => x = 3.0,8a + 2a = 0,748 mol

Chọn D.
Tại nNaOH = x mol Þ 2a + 3.0,8a = x (1)
Tại nNaOH = 0,918 mol Þ 4a – 0,6a = 0,918 – 2a (2)
Từ (1), (2) suy ra: x = 0,748 và a = 0,17
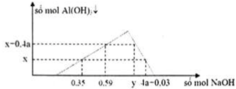




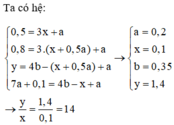
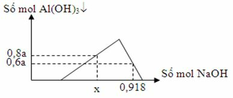

Đáp án C