Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
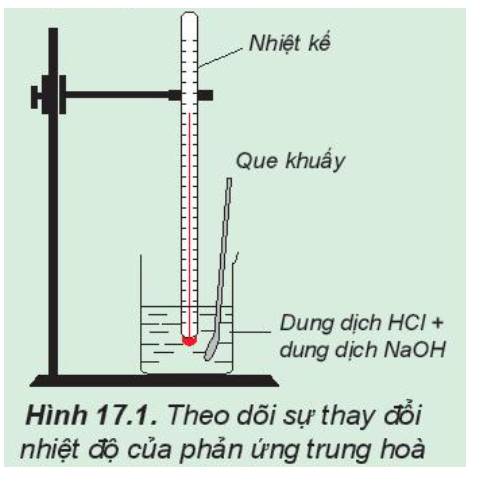
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.

\(V_{45}=0.068\)
=>\(2^3\cdot0.017=0.068\)
=>Cần giảm nhiệt độ xuống 15 độ C để tốc độ phản ứng là 0,017mol/(L.min)

Thí nghiệm 1:
2HCl + MgO → MgCl2 + H2O
=> Cốc thí nghiệm nguội dần ( HCl ban đầu hơi ấm) => Phản ứng thu nhiệt.
Thí nghiệm 2:
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
=> Cốc thí nghiệm nóng lên => Phản ứng tỏa nhiệt.

Vì bài cho hỗn hợp bazơ mà chúng có tính chất tương tự nhau nên chúng ta gộp chung 2 bazơ để cho đơn giản hơn. Với 2 khí Cl2 và Br2 thì khí Cl2 có tính oxi hóa mạnh hơn sẽ tham gia phản ứng trước
Gọi CT chung kiềm là ROH.
\(PTHH:Cl_2+2ROH\rightarrow RCl+RClO+H_2O\)
Ta có:
\(\frac{n_{Cl2}}{1}< \frac{n_{ROH}}{2}\)
Nên Cl2 hết, ta tính khối lượng muối clorua theo Cl2
Giả sử muối chỉ có NaCl
\(\Rightarrow m=0,1.58,5=5,85\left(g\right)\)
Giả sử muối chỉ có KCl
\(\Rightarrow m=0,1.74,5=7,45\left(g\right)\)
Vậy khối lượng muối clorua thu được sau phản ứng nằm trong khoảng: (5,85; 7,45)g

đặt công thức Chung của 2 bazo là XOH
\(\Rightarrow n_{XOH}=n_{NaOH}+n_{KOH}=0,4mol\)
\(m_{XOH}=m_{NaOH}+m_{KOH}=19,2g\)
=> \(M_{XOH}=48\Rightarrow M_M=31\)
Cl2 có tính oxi hóa mạnh hơn Br2 nên Cl2 phản ứng trước Br2
Vì nXOH=0,2=2nCl2 < 0,1
=> Cl2 phản ứng hết
\(2XOH+Cl_2\rightarrow XCl+XClO+H20\)
=> \(n_{XCl}=0,1mol\)
=> \(m_{XCl}=6,65g\)
bài 1: pthh:Cl2 +2ROH -> RCl+RClO+H2O
Ta có: nCl2/1 <nROH/2 ->Cl2 hết ,ta tính m muối clorua theo Cl2
giả sử muối chỉ có NaCl -> m=0,1.58,5=5,85g
giả sử muối chỉ có KCl -> m=0,1.74,5=7,45g
vậy m muối clorua thu đc sau pư trong khoảng (5,85;7,45)g
giải thích :vì bài cho hỗn hợp bazo mà chúng có tính chất tương tự nhau nên chúng ta gộp 2 bazo lại cho đơn giản .vs 2 khí Cl2 và Br2 thì Cl2 có tính oxi hóa mạnh hơn sẽ tham gia vào pư trc
Bài 2: nCl2 =22,4/22,4 =1 mol
nNaOH= 0,1.2=0,2 mol
nCa(OH)2= 0,1.0,5=0,05 mol
pthh:
2NaOH+Cl2 ->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2 +2Cl2 ->CaCl2+Ca(ClO)2 +2H2O
0,05 0,05 0,025
m=0,025.111+0,1.58,5=8,625g

Câu 5 : Cho hỗn hợp hai muối MgCO3 và CaCO3 tan trong dung dịch HCl vừa đủ tạo ra 2,24 lít khí đktc . Số mol của 2 muối cacbonat ban đầu là ?
| MgCO3 | → | MgO | + | CO2 |
CaCO3-->CaO+CO2
n hỗn hợp khí =2,24\22,4 =0,1 mol
=>nhh 2muối =0,1 mol
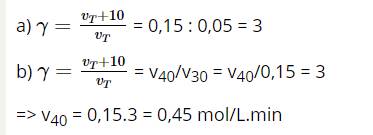
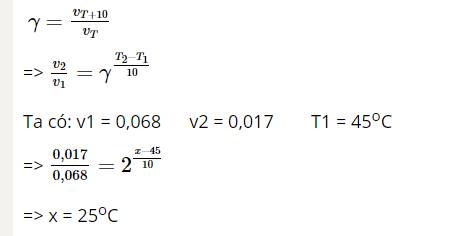



Đề có thiếu j không