Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

H : 3,7% ; P: 37,8% ; O : 58,5%.
Gọi công thức là: H x P y O z :
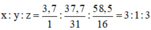
⇒ H 3 PO 3

Đặt công thức hoá học của axit là H x N y O z . Ta có :
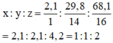
Công thức hoá học của axit là HNO 2 (axit nitrơ).

H : 2,4% ; S : 39,1% ; O : 58,5%.
Gọi công thức là H x S y O z :

⇒ HSO 3

câu a đề sai, kêu sửa đề rồi mà sao chưa sửa?
ta có H:N:O= 2.12/1 : 29.8/14 : 68.08/16
=2.12:2,128:4.225
=1:1:2
==> HNO2
b) H:P:O=3.7/1 : 37.8/31 : 58.5:16
= 3.7 :1.22 : 3.65
= 3:1:3
==> H3PO3

Bài 4. Axit axetic có công thức C2H402. Hãy tính thành phần phần trăm khối lượng của các nguyên tố trong axit axetic.
Lời giải:
Từ C2H4O2 ta có: M = 60 g/mol; mC = 2 x 12 = 24 g; mH = 4 x 1 = 4 g;
MO = 2 x 16 = 32 g.
%C = (24 : 60) x 100% = 40%; %H = (4 : 60) x 100% = 6,67%;
%O = 100% - 40% - 6,67% = 53,33%.


a) 40% S còn lại là oxi
Ta có
m\(_S:m_O=40:60\)
=>n\(_S:n_O=\frac{40}{32}:\frac{60}{16}\)
=1,25:3,75
=1:3
CTHH:SO3
b) mCu:mO=4:1
=>n\(_{Cu}:n_O=\frac{4}{64}:\frac{1}{16}\)
=0,0625:0,0625
=1:1
CTHH:CuO
c) Cứ 7g Fe kết hợp với 3g O
m\(_{Fe}:m_O=7:3\)
=>n\(_{Fe}:n_O=\frac{7}{56}:\frac{3}{16}\)
=0,125:0,1875
=12:3
CTHH"Fe2O3
d) Có 1 phần khối lượng là H và 8 phần khối lượng là O
m\(_H:m_O=1:8\)
=>n\(_H:n_O=\frac{1}{1}:\frac{8}{16}=1:0,5\)
CTHH:H2O
Chúc bạn học tốt
a, \(n_S:n_O=\frac{40}{32}:\frac{60}{16}=1:3\)
CTHH : SO3
b,
\(n_{Cu}:n_O=\frac{4}{64}:\frac{1}{16}=1:1\)
=> CTHH : CuO
c,\(n_{Fe}:n_O=\frac{7}{56}:\frac{3}{16}=2:3\)
=>CTHH: Fe2O3
d,\(n_H:n_O=\frac{1}{1}:\frac{8}{16}=1:0,5\)
=>CTHH : H2O

Câu 1 :
\(CT:P_xO_y\)
\(\%P=\dfrac{31x}{142}\cdot100\%=43.66\%\)
\(\Rightarrow x=2\)
\(M_B=31\cdot2+16\cdot y=142\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow y=5\)
\(CTPT:P_2O_5\)
\(H_xN_yO_z\\ x:y:z=\frac{1,6}{1} : \frac{22,2}{14} : \frac{76,2}{16}\\ x:y:z=1,6:1,6:4,8\\ \Rightarrow x:y:z=1:1:3\\ \Rightarrow HNO_3\\ \Rightarrow A\)